乳腺癌是女性最常见的恶性肿瘤之一。我国女性乳腺癌每年新发患者约 27 万例 [1],其中 3%~8% 初诊时即为转移性 [2]。即便是接受了手术及规范治疗的早期患者,仍有 30%~40% 会复发转移 [3]。目前肿瘤传统预后评价方式都有其局限性:
检测方式 | 优势 | 局限性 |
影像学 | 非侵入、直观对患者的肿瘤大小变化情况进行评估 | ☆辐射存在一定的健康危害或健康隐患 ☆ 肿瘤大小常与肿瘤的恶性程度或浸润能力不完全一致 ☆ 费用昂贵 ☆ 滞后性 ☆ 灵敏性低 |
血清学 | 微创,血清肿瘤标志物的浓度往往可以在一定程度上提示肿瘤的发展程度 | ☆ 特异性差 ☆ 易受非特异蛋白的干扰 ☆ 其他的病理生理状态影响导致假阳/阴性结果 |
病理学 | 目前唯一明确肿瘤有否转移的金标准 | ☆ 精确度不够高 ☆ 侵入性检查手段,易造成扩散 ☆ 人工误差大 ☆ 难以标准化 |
随着遗传学、分子病理学的发展,乳腺癌诊疗已经步入分子分型指导下的个体化诊疗时代。2018 年 1 月 1 日在全球启用的 AJCC 第八版癌症分期系统,将乳腺癌外周血中的循环肿瘤细胞(circulating tumor cell,CTC)列为预后提示因子,上皮-间质转化 (epithelial-mesenchymal transition,EMT) 参与了癌症的转移过程,因此临床对基于 EMT 标志物的 CTC 分型检测提出需求。尽管有证据表明基于 EMT 标志物的 CTC 异质性与疾病进展相关,但临床实践尚无标准建议。
近日,国家癌症中心在国际著名癌症期刊《癌症通讯》在线发表了基于上皮-间质转化标志物的 CTC 分型检测对 HER-2 阴性转移性乳腺癌一线化疗的预后意义。

该研究由国家癌症中心/国家癌症临床研究中心、中国医学科学院北京协和医学院肿瘤医院管秀雯、马飞、王佳玉、罗扬、蔡锐刚、樊英、李俏、陈闪闪、张频、李青、徐兵河等学者共同完成,本次研究采用益善生物 CanPatrol® CTC 富集技术对 108 例 HER2 阴性转移性乳腺癌患者(患者均来自 CAMELLIAⅢ期前瞻性研究)外周血中 CTC 进行富集并鉴定其型别(包括上皮型、混合型和间质型)。研究表明:结合 CTC 总数和间质型 CTC 比例的标准,可用于转移性乳腺癌患者的治疗耐药性和预后监测;同时明确了无进展生存期(PFS)预测联合标准:CTC 总数 ≥ 10/5 mL、间质型 CTC 比例>10.7%,符合联合标准的患者 PFS 中位数明显比不符合标准的患者短(6.2 vs 9.9 月,P = 0.010)。
为该项目提供技术支持的益善生物是我国专注肿瘤实时个体化医疗检测产品研发、生产和推广的国家级高新科技企业。同时,其自主研发的 Canpatrol® CTC 分型检测技术采用不依赖于特定标志物的 CTC 分离方式,有机结合了纳米技术和多重 RNA 原位分子技术优势,同步实现了 CTC 的分离、分型和分析。益善生物致力于在肿瘤实时动态监测、实时疗效评估和实时个体治疗药物选择等领域构筑系统解决方案。
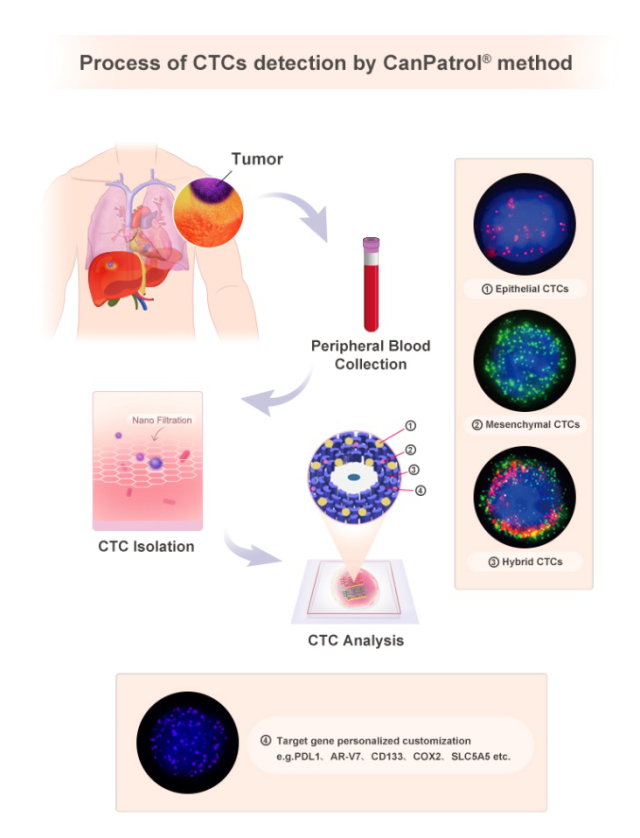
图片来源:益善生物
参考文献
[1] Chen W, Zheng R, Baade P D, et al. Cancer statistics in China, 2015[J]. CA: a cancer journal for clinicians, 2016, 66(2): 115-132.
[2]Slegel R L, Miller K D, Jemal A. Cancer Statistics. 2016[J]. CA Cancer J Clin, 2016, 66(1): 7-30.
[3]Gonzalez-Angulo A M, Morales-Vasquez F, Hortobagyi G N.Overview of resistance to systemic therapy in patients with breast cancer[J].Adv Exp Biol,2007,608:1-22.
阅读原文:点击下载 PDF 文件
