近日,中国抗癌协会乳腺癌专业委员会发布了最新版的《中国抗癌协会乳腺癌诊治指南与规范(2017 版)》,现将其整理成「快速上手指南」,方便查看与学习。
乳腺癌筛查
1. 筛查年龄:机会性筛查一般建议 40 岁开始, 但对于一些乳腺癌高危人群,可将筛查起始年龄提前到 40 岁以前。
乳腺癌高危人群:有明显的乳腺癌遗传倾向者;既往有乳腺导管或小叶不典型增生或小叶原位癌的患者;既往行胸部放疗。
2. 筛查方法: X 线检查、乳腺超声检查 、MRI 检查。
浸润性乳腺癌保乳治疗
1. 外科手术
适应证:临床 I 期、II 期的早期乳腺癌和 III 期非炎性乳腺癌。
绝对禁忌证:(1)妊娠期间放疗;(2)病变广泛或弥漫分布的恶性特征钙化灶,且难以达到切缘阴性或理想外形;(3)肿瘤经局部广泛切除后切缘阳性,再次切除后仍不能保证病理切缘阴性者;(4)患者拒绝行保留乳房手术;(5)炎性乳腺癌。
2. 术后放疗
(1)放疗剂量:全乳照射剂量 45~50 Gy,1.8~2.0 Gy/次,5 次/周。在无淋巴引流区照射的情况下也可考虑大分割方案治疗, 即 2.66 Gy×16 次, 总剂量 42.5 Gy。在全乳照射基础上可通过瘤床加量进一步提高局部控制率,剂量为 (10~16) Gy/(1~1.5) 周, 共 5~8 次。
(2)与全身治疗的时序配合:无辅助化疗指征的患者放疗建议在术后 4~8 周内进行;接受辅助化疗的患者应在末次化疗后 2~4 周内开始。
乳腺癌前哨淋巴结活检(SLNB)
SLNB 是早期浸润性乳腺癌的标准腋窝分期手段。
适应证:早期浸润性乳腺癌;临床腋窝淋巴结阴性;单灶或多中心性病变;导管内癌接受乳房切除术;临床腋窝淋巴结阴性新辅助治疗后。
禁忌证:炎性乳腺癌;腋窝淋巴结穿刺证实为转移且未接受新辅助治疗;腋窝淋巴结阳性新辅助治疗后仍为阳性。
乳腺癌全乳切除术后放疗
1. 适应证:(1)原发肿瘤最大直径大于等于 5 cm,或肿瘤侵及乳腺皮肤、胸壁;(2)腋窝淋巴结转移大于等于 4 枚;(3)淋巴结转移 1~3 枚的 T1-2;(4)T1-2 乳腺单纯切除术,如 SLN 阳性,当不考虑后续腋窝清扫时,推荐术后放疗;如不考虑放疗,则推荐进一步腋窝清扫。
2. 放疗剂量:共 50 G y(5 周,25 次)的剂量, 可考虑局部加量至 60~66 Gy。
3. 与全身治疗的时序配合:应在完成末次化疗后 2~4 周内开始。
乳腺癌全身治疗
1. 术后辅助全身治疗

(1)化疗方案
常用的有:① 以蒽环类为主的方案, 如 CAF、A(E)C、FEC 方案(C:环磷酰胺,A:多柔比星,E:表柔比星,F:氟尿嘧啶);② 蒽环类与紫杉类联合方案, 如 TAC(T:多西他赛);③ 蒽环类与紫杉类序贯方案, 如 AC→T/P(P:紫杉醇)或 FEC→T;④ 不含蒽环类的联合化疗方案, 适用于老年、低风险、蒽环类禁忌或不能耐受的患者, 常用的有 TC 方案及 CMF 方案(M:甲氨蝶呤)。
中国专家团认为三阴性乳腺癌的优选化疗方案是含紫杉和蒽环的剂量密度方案。
(2)内分泌治疗
绝经前:① 他莫昔芬,治疗期间注意避孕,并每 6~12 个月行 1 次妇科检查,通过 B 超检查了解子宫内膜厚度;② 卵巢功能抑制加他莫昔芬;③ 卵巢功能抑制加第三代芳香化酶抑制剂。
绝经后:第三代芳香化酶抑制剂可以向所有绝经后的 ER 和(或)PR 阳性患者推荐,尤其是具备以下因素的患者:① 高复发风险患者;② 对他莫昔芬有禁忌的患者或使用他莫昔芬出现中、重度不良反应的患者;③ 使用他莫昔芬 20 mg/d×5 年后的高风险患者。
(3)术后辅助曲妥珠单抗治疗
适应证:原发浸润灶大于 1.0 cm HER-2 阳性时, 推荐使用曲妥珠单抗;原发肿瘤在 0.5~1.0 cm 时,可考虑使用。
治疗方案:曲妥珠单抗 6 mg/kg(首次剂量 8 mg/kg)每 3 周方案,或 2 mg/kg(首次剂量 4 mg/kg)每周方 案。时间为 1 年,可与化疗同时使用或化疗后序贯使用。
2. 新辅助治疗
适合临床 II、III 期的乳腺癌患者:① 临床分期为 IIIA(不含 T3、N1、M0)、 IIIB、IIIC 期;② 临床分期为 IIA、IIB、IIIA(仅 T3、 N1、M0)期,对希望缩小肿块、降期保乳的患者,也可考虑新辅助治疗。
常用的含蒽环类和紫杉类药物的联合化疗方案:① 以蒽环类为主的化疗方案, 如 CAF、 FAC、AC、CEF 和 FEC 方案;② 蒽环类与紫杉类联合方案, 如 A(E)T、 TAC; ③ 蒽环类与紫杉类序贯方案,如 AC→P 或 AC→T;④ 其他化疗方案, 如 PC(C: 卡铂)。
3. 晚期乳腺癌解救性全身治疗
(1)化疗
推荐首选化疗方案包括单药序贯化疗或联合化疗。
常用单药包括: 蒽环类、紫杉类、抗代谢药(如卡培他滨、吉西他滨)、非紫杉类微管形成抑制剂(如长春瑞滨、艾日布林)。
常用的联合化疗方案包括:FAC、FEC、CTF、AC、EC、AT、CMF、多西他赛联合卡培他滨、吉西他滨联合紫杉醇。对于三阴性乳腺癌, 可选择吉西他滨加卡铂或顺铂。
其他有效的单药还包括:环磷酰胺、顺铂、口服依托泊苷、长春花碱、米托蒽醌和氟尿嘧啶持续静脉给药方案。
(2)内分泌治疗
① 尽量不重复使用辅助治疗或一线治疗用过的药物;② 他莫昔芬治疗失败的绝经后患者可选氟维司群(500 mg)或芳香化酶抑制剂;③ 一类芳香化酶抑制剂治疗失败患者可选另外一类芳香化酶抑制剂(加或不加依维莫司)或氟维司群(500 mg),若未证实有他莫昔芬抵抗,也可选用他莫昔芬;④ ER 阳性的绝经前患者可采取卵巢手术切除或其他有效的卵巢功能抑制治疗, 随后遵循绝经后妇女内分泌治疗指南;⑤ 二线内分泌治疗之后的内分泌治疗, 应选择既往内分泌治疗获益的药物。
(3)HER-2 阳性的晚期乳腺癌治疗
一线治疗:曲妥珠单抗可联合的化疗药物和方案有紫杉醇联合或不联合卡铂、多西他赛、长春瑞滨和卡培他滨, 以及联合多西他赛 + 帕妥珠单抗。
二线治疗:① 可保留曲妥珠单抗,而更换其他化疗药物,如卡培他滨;② 也可换用拉帕替尼加用其他化疗药物,如卡培他滨;③ 也可停用细胞毒药物,而使用两种靶向治疗药物的联合,如拉帕替尼联合曲妥珠单抗,或帕妥珠单抗联合曲妥珠单抗(目前尚未在国内进行临床试验);④ 也可考虑使用 TDM-1。
4. 终末期姑息治疗
(1)疼痛:三阶梯止痛。为了达到 4A 目标,近年指南将小剂量三阶梯药物(如每日剂量小于等于 30 mg 的吗啡和每日剂量小于等于 20 mg 的羟考酮)划分到第二阶梯,临床上可用小剂量三阶梯药物处理中度癌痛。
(2)厌食和恶液质:建议以肠内营养为主,为纠正水电解质异常或肠内营养不足,可适当进行静脉营养,此外固醇类皮质激素、孕激素(甲地孕酮、甲羟孕酮)及胃动力药物等可适当作为辅助治疗。
(3)恶心呕吐:针对原因进行治疗,如放疗和化疗前预防性给予止吐药物、脑转移者给予脱水、胃肠道梗阻者给予胃肠减压等处理
(4)疲乏:治疗一般先针对病因(如止痛、抗感染及保护心、肝、肾功能),纠正不足(如水电解质、血糖、红细胞、白细胞、血小板及血氧),支持治疗中可考虑加用一些皮质激素如地塞米松或孕激素甲地孕酮、甲羟孕酮, 也可佐以精神兴奋剂如哌甲酯。
(5)昏迷:① 病因治疗;② 支持治疗:保证糖分和营养适度, 维持静脉通路, 纠正酸碱失衡, 保持水和电解质的平衡;③ 加强护理 。
乳腺癌原位(内)癌治疗(DCIS)
1. 局部治疗
(1)外科治疗:全乳切除术对 98% 的 DCIS 患者是一种治愈性方法。 近来的研究发现, 肿块切除(不包括腋窝淋巴结清扫)+全乳放疗与乳房切除术有相似的生存率。
(2)放疗:保乳手术后行全乳放疗可以降低约 50% 的同侧复发风险。
2. 系统治疗
以下情形考虑采用他莫昔芬治疗 5 年以降低保乳手术后同侧乳腺癌复发风险:(1)接受保乳手术(肿块切除术)加放疗的患者, 尤其是 ER 阳性的 DCIS 患者;ER 阴性的 DCIS 患者他莫昔芬治疗效果尚不确定。(2)仅接受保乳手术的患者。
HER-2 阳性复发转移乳腺癌的治疗
曲妥珠单抗治疗后的疾病进展治疗策略:1. 拉帕替尼联合卡培他滨 ;2. 曲妥珠单抗联合卡培他滨;3. 还可以考虑曲妥珠单抗联合拉帕替尼的方案,尤其对经多线治疗后的患者仍可有效;4. 继续使用曲妥珠单抗, 更换其他化疗药物。
乳腺癌局部和区域淋巴结复发的治疗
1. 放疗
全胸壁和区域淋巴结照射剂量达到 50 Gy(共 25 次)或相应的生物等效剂量后,对复发灶需要加量至 60 Gy, 对未切除的复发灶照射剂量需要在 60 Gy 以上, 必须控制正常组织损伤。
2. 全身治疗
下列情况需要考虑全身治疗:局部-区域病变较大或不可切除,但经全身治疗后病变缓解有可能变得可以切除者;孤立的局部区域复发在得到有效的局部治疗后,巩固化疗有可能改善 PFS 和 OS,应考虑化疗,尤其是复发病灶对内分泌治疗不敏感或无效者;激素受体阳性患者内分泌治疗,具有可持续治疗和降低再次复发率的价值;复发灶广泛乃至放射治疗难以覆盖完整的靶区; 同期放化疗可以提高局部控制率;HER-2 阳性患者可以联合靶向治疗。与其他复发转移患者的治疗原则一致,应密切跟踪治疗方案的疗效,并适时调整治疗方案。
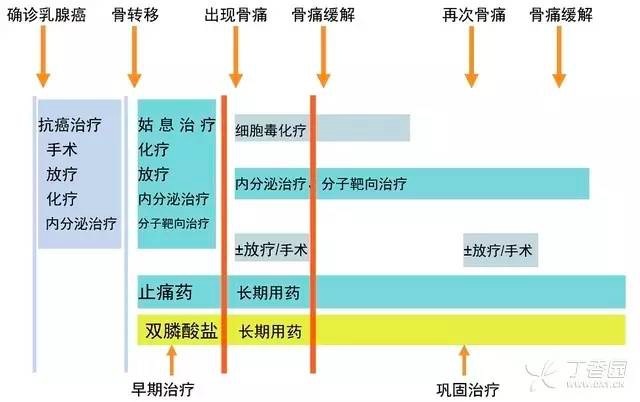
乳腺癌骨转移的治疗