2021 年 9 月 6 日,中山大学肿瘤防治中心徐瑞华教授、王峰教授团队在消化道领域权威期刊《Gut》上发表文章,阐述 ctDNA 动态监测在不可切除转移性结直肠癌患者预后评估中的作用。该研究基于超微量液体活检技术进行了 ctDNA 超低频突变检测,海普洛斯许明炎博士、陈实富博士为论文共同作者。

该研究纳入了 171 名接受一线治疗、不可切除的转移性结直肠癌患者,并对患者治疗前后进行了动态 ctDNA 检测。研究展示出结直肠癌患者基因突变图谱在时间上的异质性。有趣且非常具有临床价值的发现是,肿瘤患者 ctDNA 中 RAS 和 BRAF 基因突变状态的改变伴随着临床预后上的显著改变。这打破了传统认为肿瘤患者最初的突变状态决定了其预后的观点,说明对转移性结直肠癌患者进行 ctDNA 动态监测在预后预测上的临床必要性。
背景介绍:
结直肠癌是全球第二大常见癌症,并且在许多国家仍有增加趋势。结直肠癌也是癌症相关死亡的第二大主要原因,其五年死亡率约为 40%。随着分子诊断技术的发展,转移性结直肠癌患者的诊治方案得到了很大改进,目前有多类治疗策略,包括化疗、靶向和免疫治疗。在用药指导和预后预测方面,肿瘤患者体细胞突变检测对于结直肠癌患者病程管理具有至关重要的作用。比如,RAS 基因家族(包括 KRAS、NRAS、HRAS)或者 BRAF V600E 发生体细胞突变会对西妥昔单抗的治疗产生耐药,并且是预后不良的指标。以循环肿瘤 DNA(circulating tumor DNA, ctDNA)为检测对象的液体活检技术具有实时、动态、全面和无创的特点,因此在癌症基因组检测领域得到了广泛应用,可用于结直肠癌患者全病程管理,比如早期诊断、微小残留病灶检测、治疗靶点检测和疗效监测等。
针对接受一线治疗的转移性结直肠癌患者,直接和实时预测患者预后的好坏,可以及时地调整患者的治疗策略,减少不必要的毒副作用。而在用药指导方面,最近也有研究表明:具有 RAS 家族基因突变的转移性结直肠癌患者,在后续 ctDNA 检测显示 RAS 家族基因突变消失的,可以接受抗 EGFR 治疗。因此,通过实时、动态监测 ctDNA 中的生物标记物,对接受一线治疗的转移性结直肠癌患者的预后进行预测,具有重要的临床意义和应用前景。
研究路线:
从 2018 年 4 月到 2020 年 1 月,共有 171 名不可手术切除的转移性结直肠癌患者入组。收集患者原发肿瘤组织和一线治疗前外周血样本,进行肿瘤组织全外显子测序 (63 例) 和 ctDNA 的 HaploX 378-gene panel 靶向捕获测序(171 例),以此作为基线。并从一线治疗开始,每 6-8 周收集患者的连续血液样本,进行 ctDNA HaploX 378-gene panel 靶向捕获测序,同时根据《实体肿瘤的反应评价标准》(RECIST)V1.1 对受试者的临床疗效及肿瘤负荷进行临床反应评估,直至疾病进展或最后一次随访。
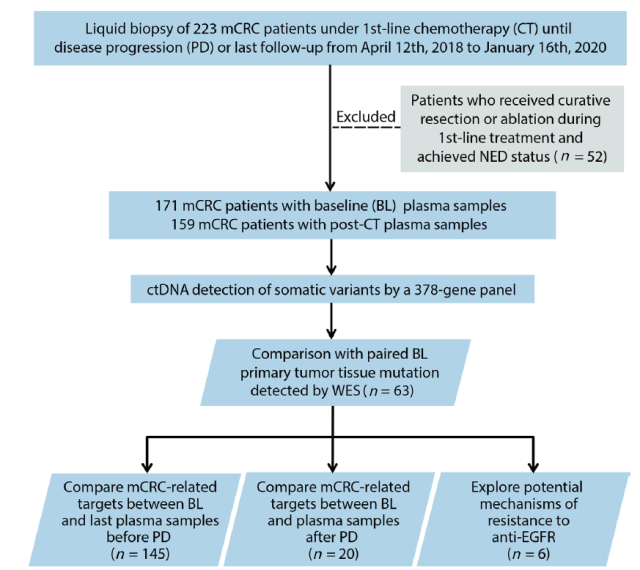
图 1. 试验设计和患者选择流程图
研究结果:
1. 肿瘤患者基线 ctDNA 和肿瘤组织突变一致性
对于接受系统性一线治疗的转移结直肠癌患者,治疗前血浆 ctDNA 和肿瘤组织突变图谱显示出非常好的一致性,其中 RAS 和 BRAF V600E 突变的一致率为 81% (51/63),说明 ctDNA 作为实时监测肿瘤基因突变材料的可靠性。
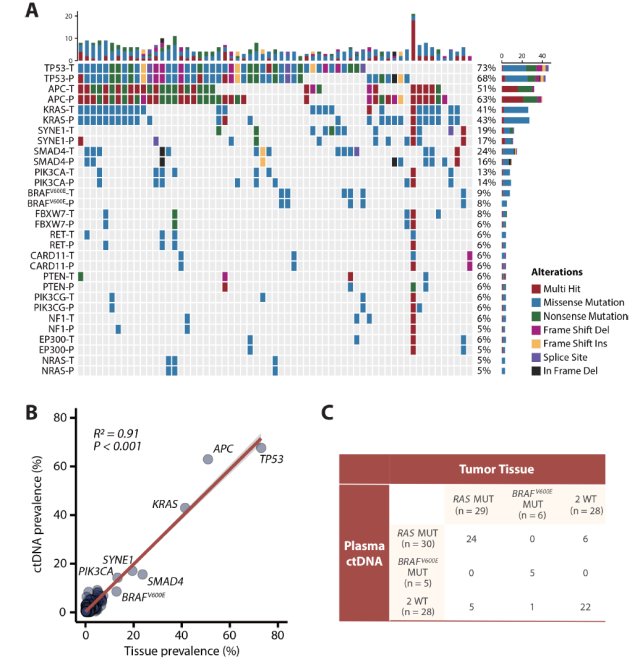
图 2. 63 名肿瘤患者基线 ctDNA 和肿瘤组织突变一致性分析
2. 一线治疗过程中,ctDNA 基因突变的进化过程
对 171 例患者 ctDNA 进行长期多时间点动态监测,分析得到了 ctDNA 中的高频突变基因频谱,并关注了与结肠癌(Colorectal cancer,CRC)相关的临床标准治疗(standard-of-care,SOC)、临床试验中 (clinical trial) 的相关靶点。在 SOC 中,42.6% (26/61) 基线携带有 RAS 突变的患者在标准治疗过程中突变被清除,50%(5/10)的 BRAF 突变患者在标准治疗过程中突变被清除;相反,3.6% (3/84) 和 0.7% (1/135) 的患者的 ctDNA 分别显示了新的 RAS 突变及 BRAF 突变。
此外,1/3 的患者发生了 ERBB2 扩增的清除,却无患者重新获取 ERBB2 扩增这种突变。与 SOC 靶标不同,临床试验相关靶点,包括 KRASG12C, BRAFnonV600E, PTEN, NF1, MTOR, CDK12, CDKN2A, FGFR1/FGFR2/FGFR3 等突变的状态改变总计仅发生在 12.4% (18/145)的患者中,随时间变化前后基本一致,无明显变化。
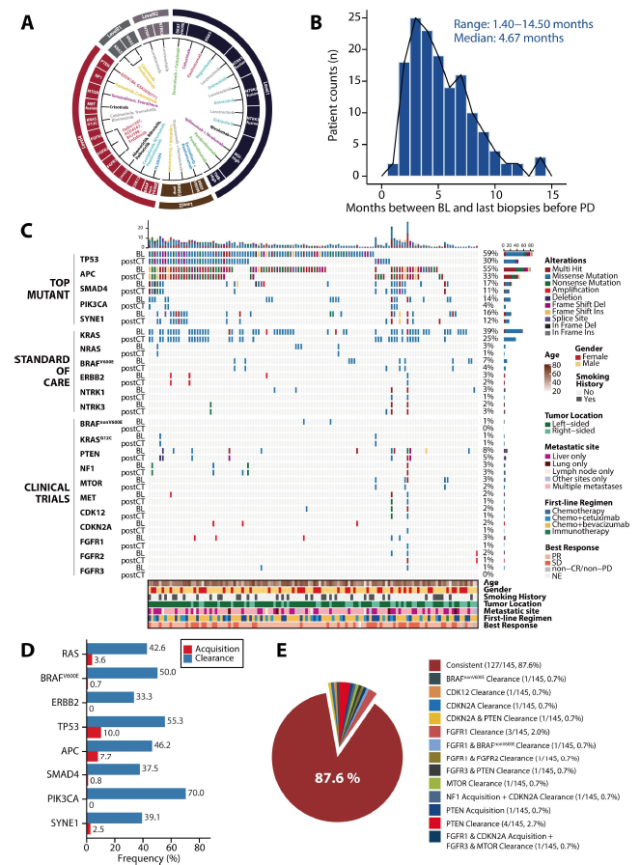
图 3. 一线治疗过程,145 名患者基因组在时间上的异质性
3. ctDNA 中 RAS 与 BRAFV600E 的变化与临床结果的相关性
有趣且具有临床相关性的发现是,转移性结肠癌(metastatic colorectal cancer,mCRC)患者 ctDNA 中 RAS 和 BRAF 基因突变状态的改变伴随着临床预后(PFS 和 OS)的显著变化。RAS 或 BRAF 清除患者的中位无进展生存期 (mPFS) 分别为 12.8 个月 (95%CI 10.2 ~ 未达到 (NR)) 和 NR (95%CI 18.9 ~ NR),这与无 RAS 或 BRAF 突变的患者的 mPFS 结果一致(其中无 RAS 突变是 13.2 月 (95%CI 10.8 ~ 16.4; p = 0.980);无 BRAF 突变 11.5 月 (95%CI 10.4~13.3; p = 0.196))),但其 mPFS 的结果仍显著优于有 RAS 突变(7.9 月; 95%CI 5.1~ 10.9; p = 0.002)或 BRAF 突变(6.4 月; 95%CI 3.2~ NR; p = 0.002)的患者。相反的,新发生 RAS 或 BRAF 突变的患者的 mPFS 分别为 6.1 个月和 8.7 个月,这和起初伴有 RAS 或 BRAF 突变的患者预后相当,均差于始终无 RAS 或 BRAF 的患者。
总的来说,当 RAS 或者 BRAF 基因由突变型转变为野生型时,患者疗效改善,且预后好。这表明患者肿瘤最初的突变状态并不能作为可靠的预后分类和治疗决策依据。实际上,一线治疗过程中的突变状态可能对患者的疗效和预后影响更大。同样,在一线系统治疗失败时,研究人员也观察到显著的体细胞突变图谱变化。这不仅能够部分解释治疗失败的原因,并且为后续治疗提供更多有效信息。
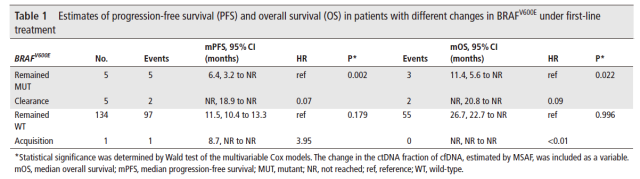
表 1. RAS 或 BRAF 状态改变的患者的 PFS 与 OS
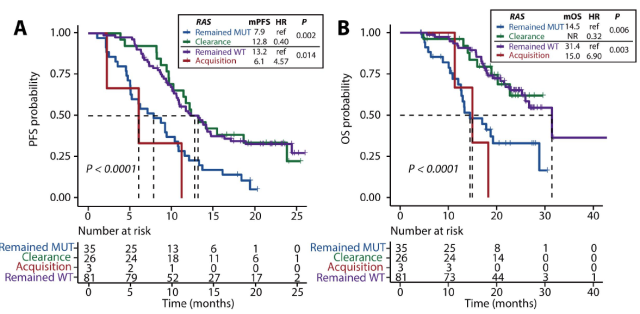
图 4. 根据一线治疗过程中 ctNDARAS 状态改变来分类的患者的无进展生存期 (PFS) 和总生存期 (OS)
讨论与总结:
在该项研究中,我们首先发现了肿瘤组织和血浆 ctDNA 在检测体细胞突变时高度的一致性,说明使用 ctDNA 在 mCRC 的综合治疗中用于检测的可靠性。研究结果为 ctDNA 可以用代替组织指导临床方案提供了更为坚实的证据,尤其是在反复组织活检不可行的情况下。在实际临床场景中,后续的临床判断如果依赖于历史保存的组织样本,不能够及时反映后续病人的突变情况。相比下,ctDNA 可以用来实时动态监测患者的突变情况,尤其是在患者治疗失败需要重新面对新的治疗方案时。
在 mCRC 的一线治疗中,我们发现体细胞突变状态会发生变化,也反应了 ctDNA 监测在临床决定的必要性。近期其他研究表情,mCRC 患者 RAS 突变的清除可以用作 EGFR-rechallenge 的生物标记物,然而在患者发生疾病进展(PD)前,RAS 的变化还鲜有研究。本研究更多注重 PD 前 RAS 的变化,并且发现 RAS 清除率高达 42.6% (26/61)。
更为重要的是,ctDNA 中 RAS 或 BRAF 突变情况的变化与预后有直接的相关性。发生 RAS 或 BRAF 突变到野生型的患者有更长的无进展生存期(PFS)和总生存期(OS),而由野生型 RAS 或 BRAF 转变为突变型的 RAS 或 BRAF 的患者有更差的预后。这也说明完全以患者起初的突变状态作为预后标志物及临床方案的依据并不总是可靠。
本研究为一项大规模前瞻性和观察性临床试验, 绘制了转移性结直肠癌患者在一线治疗中 ctDNA 动态基因突变图谱,为利用 ctDNA 测序技术来捕获肿瘤基因变异提供了有力证据,同时也显示出肿瘤在时间上的异质性。本研究还发现肿瘤患者 RAS 和 BRAF 基因突变状态变化伴随着预后的明显改变,这在临床实践中应该引起足够重视。
参考文献:http://dx.doi.org/10.1136/gutjnl-2021-324852
专家介绍:

徐瑞华 MD, PhD 教授,博士生导师、结直肠癌内科首席专家
中山大学附属肿瘤医院
中山大学肿瘤防治中心院长、所长,华南肿瘤学国家重点实验室主任,肿瘤医学省部共建协同创新中心主任,国家新药(抗肿瘤药物)临床试验中心主任。长期从事肿瘤内科临床工作,在消化系统肿瘤治疗、早诊筛查、转移耐药方面做出国际先进的创新性成果:1. 在国际上首创了多种晚期胃肠肿瘤的治疗方案,建成了结直肠癌全程治疗新体系,优化了分子标志物指导下的晚期胃癌靶向治疗策略,多项研究结果被美国 NCCN 指南引用,成为新的国际标准。2. 应用 ctDNA 甲基化技术及人工智能辅助内镜技术等提高了消化系统肿瘤的早诊率。3. 肿瘤转移耐药研究取得突破,创新了分子标志物指导下的免疫治疗策略,明显提高了疗效,并推动了我国新药临床研究发展。研究成果大幅延长了晚期胃癌、肠癌患者的总生存时间,所治疗病患的 5 年生存率达国际领先水平。
研究结果被写入多部国际指南和英文经典专著,在全世界推广应用;连续入选了中国高被引学者;担任国家研究生统编教材《肿瘤学》主编;以第一完成人获 2 项国家科技进步二等奖及 6 项省部级科技进步一等奖(2 项中华医学科技奖一等奖、2 项广东省科技进步一等奖及 2 项教育部高等院校科学研究优秀成果一等奖)。
以通讯或第一作者发表高水平论文 167 篇,有多篇文章发表在国际上重要的学术期刊上,如《Nature Materials》、《Lancet Oncology》、《Journal of Clinical Oncology》、《JAMA Oncology》等。

王峰 MD, PhD,主任医师,内科副主任
中山大学附属肿瘤医院 肿瘤内科
美国 MD Anderson 肿瘤中心博士(PhD)、中山大学临床医学博士(MD)。共发表高水平论文 60 篇,包括 30 篇以第一(含共一)或通讯(含共通讯)作者发表于知名期刊 JAMA Oncology (2019, IF:22.4)、Cell Research (2018, IF:17.8)、Annals of Oncology (2019, IF:14.2) 等,13 篇 IF > 5,其中 3 篇 IF >10。相关研究成果被写入 NCCN 指南,近五年作为课题负责人承担了科研基金共 10 项,包括国家自然科学基金 2 项,参与 863 计划等科技项目 9 项。2016 获珠江科技新星,荣获国家科技进步奖二等奖(排名 2/10)、中华医学科技一等奖(排名 3/15)等科研奖励。申请国内发明专利 4 项,已获得授权 1 项。获邀在美国肿瘤研究协会年会(AACR)、中国临床肿瘤学会年会(CSCO)等做口头报告。
