2013 年欧洲肿瘤医学会(ESMO)发布了《新诊断和复发的上皮性卵巢癌诊断、治疗及随访的临床实践指南》。随着相关证据的增加及更新,其于 2021 年 7 月对其进行了更新。
本次更新主要聚焦在新诊断上皮性卵巢癌的一线维持治疗。

1 现有证据
目前主要有 4 项重要的临床研究探讨了上皮性卵巢癌的一线维持治疗,所有试验均显示患者的无进展生存期(PFS)得到了显著地改善。
其中有 3 项III期试验(SOLO-1、PAOLA-1/ENGOT-ov25 和 PRIMA/ENGOT-ov26)探讨了多腺苷二磷酸多聚酶(PARP)抑制剂(奥拉帕利或尼拉帕利)在新诊断的高级别上皮性卵巢癌(包括输卵管和腹膜癌)在手术和化疗(ChT)后的维持治疗。
在另一项试验(VELIA/GOG-3005)中,维利帕利与 ChT 联合给药,然后再进行维利帕利维持治疗。
SOLO1
SOLO1 评估了具有 BRCA 突变且对铂类化疗有完全或部分反应的 FIGO III-IV 期卵巢癌患者进行为期 2 年的单药一线维持治疗的疗效。
SOLO1 的初步结果显示,与安慰剂相比,奥拉帕利维持治疗可将疾病进展的风险显著降低 70%(HR=0.30,95%CI:0.23-0.41,P<0.001)。
长期随访也证明了获益是长期存在的。5 年随访显示奥拉帕利的中位 PFS 为 56 个月,而安慰剂为 14 个月(HR=0.33,95%CI:0.25-0.43)。5 年时,接受奥拉帕利治疗的患者中有 48% 仍无进展,而安慰剂组为 21%。
奥拉帕利已被欧洲药品管理局(EMA)和美国食品和药物管理局(FDA)批准作为 BRCA 突变患者基于铂类化疗后的一线维持治疗。
PRIMA/ENGOT-ov26
PRIMA/ENGOT-ov26 评估了尼拉帕利作为有治疗失败高风险的 III-IV 期卵巢癌患者(伴或不伴 BRCA 突变)长达 3 年的维持治疗。研究排除了初始细胞减灭术后无病灶残留的III期卵巢癌患者,有 67% 的患者接受了新辅助化疗。基于Myriad myChoice® 测定法,根据肿瘤的同源重组修复缺陷(HRD)(HRD 评分≥ 42 分)状态对患者进行了分层。研究主要对 HRD 人群进行了分析,其次是对整体人群。
该研究显示 HRD 人群(HR=0.43,95%CI:0.31-0.59,P<0.001)和整人群(HR=0.62,95%CI:0.50-0.76,P<0.001)的 PFS 都得到了显著的改善。探索性的亚组分析显示,具有 BRCA 突变的女性获益最大,BRCA 野生型的 HRD女性也显著获益,但少于前者。HRD 阴性(或称之为 HRP)人群的中位 PFS 也增加了 2.7 个月(HR=0.68,95%CI:0.49-0.94,P=0.020)。
尼拉帕利已被 EMA 和美国 FDA 批准作为所有卵巢癌患者铂类化疗后的一线维持治疗。
PAOLA-1/ENGOT-ov25
在 PAOLA-1/ENGOT-ov25 试验中,手术后有或没有残留病灶的 III-IV 期卵巢癌患者接受 ChT 联合贝伐单抗治疗,ChT 后随机接受奥拉帕利片或安慰剂维持治疗 2 年,并且两组均完成 15 个月的贝伐单抗治疗。该研究包括所有在手术后没有残留病灶并达到 NED(无疾病证据)或在 ChT 联合贝伐单抗后达到完全或部分反应的患者。根据肿瘤 BRCA 突变状态和对一线治疗的反应对奥拉帕利或安慰剂的随机化进行了分层。
对所有入组意向治疗(ITT)人群的初步分析显示,接受奥拉帕利和贝伐单抗治疗患者的 PFS 显著获益,中位 PFS 为 22.1 个月,而安慰剂和贝伐单抗治疗的中位 PFS 为 16.6 个月(HR=0.59,95%CI:0.49-0.72,P<0.001)。探索性亚组分析显示,BRCA 突变女性(HR=0.31,95%CI:0.20-0.47)的获益最大,其次是 HRD 阳性女性(使用 Myriad myChoice® 测定的 HRD≥42分)(其中包括了 BRCA 突变者)(HR=0.33,95%CI:0.25-0.45)和 BRCA 野生型的 HRD 阳性女性(HR=0.43,95%CI:0.28-0.66)。在 HRD 阴性/未知的人群中未观察到任何获益。
奥拉帕利已被 EMA 和美国 FDA 批准与贝伐单抗联合用于 BRCA 突变及 HRD 的卵巢癌患者在基于铂类化疗后的一线维持治疗。
VELIA/GOG-3005
在 VELIA/GOG-3005 试验中,将 III-IV 期卵巢癌的标准 ChT 与在 ChT 期间给予维利帕利然后再用维拉帕利维持治疗 2 年或与仅在 ChT 期间给予维利帕利治疗者进行了比较。
分层分析显示 BRCA 突变患者的进展或死亡风险最大降低 56%(HR=0.44,95%CI:0.28-0.68,P<0.001),其次是 HRD(使用Myriad myChoice®测定的HRD≥33分)患者为 43%(HR=0.57,95%CI:0.43-0.76,P<0.001)和ITT人群中的 32%(HR=0.68,95%CI:0.56-0.83,P<0.001)。ITT 人群中维利帕利和对照组的中位 PFS 分别为 23.5 和 17.3 个月。
维利帕利的一线治疗还尚未获得批准。
综上所述,所有四项试验都表明,PARP 抑制剂一线维持治疗的中位 PFS 均有获益,在具有 BRCA 突变的女性中获益最大。

2 更新的建议
所有高级别卵巢癌患者在诊断时都应进行 BRCA1 和 BRCA2 突变(胚系/体系)的检测(I,A)。
具有 BRCA 突变且对一线铂类 ChT 有部分或完全反应的患者应接受 PARP抑制剂维持治疗(奥拉帕利 2 年, 尼拉帕利 3 年)。一线 ChT 时加入了贝伐单抗者,应联合使用奥拉帕利和贝伐单抗,尽管目前尚不清楚联合用药是否会比单独使用奥拉帕利更好(I,A)。
推荐进行基因组不稳定性(HRD)检测。这样可以鉴别出那些 BRCA 野生型,但可以从 PARP 抑制剂中获益更大的女性亚组(I,A)。HRD 检测阳性且对一线含铂 ChT 有部分或完全反应者,无论是否使用贝伐单抗,都应接受 PARP 抑制剂的维持治疗,如使用奥拉帕利/贝伐单抗(如果 ChT 时使用了贝伐单抗)或尼拉帕利单药(I,A)。
一线 ChT 时使用了贝伐单抗,且 HRD 阴性的患者,在贝伐单抗维持治疗时加入奥拉帕利不会获得 PFS 获益(I,B)。这不是许可的适应症,因此不予推荐。
尼拉帕利单药治疗已获准用于所有对 ChT 有反应的 III-IV 期卵巢癌患者。由于尚无长期结果数据,因此在 HRD 阴性人群中或在 HRD 状态不明的情况下,决定将该药作为一线还是二线维持治疗,需要根据患者的具体情况而定(I,C)。
指南对 PARP 抑制剂在卵巢癌一线维持治疗中的推荐是基于现有的试验证据,但是各种 PARP 抑制剂的适应证在各个国家可能是不同的。
卵巢癌一线治疗后的奥拉帕利单药维持治疗已获批用于 BRCA 突变的女性。在许多国家,它还获批与贝伐单抗一起用于 HRD( BRCA 突变或 BRCA 野生型)的肿瘤人群。
在许多国家中,无论生物标志物状态如何,尼拉帕利都已批准作为对一线治疗有反应的 III-IV 期卵巢癌患者的单药维持治疗。
需要注意的是,目前尚不清楚在这些试验的安慰剂组中随后使用 PARP 抑制剂对总生存期(OS)的影响,因此随后的研究应着重对 OS 的评估。
此外,口服 PARP 抑制剂的不良反应在大多数患者中是可控的,但一些罕见的严重不良事件(如急性髓系白血病/骨髓增生异常)略有增加。
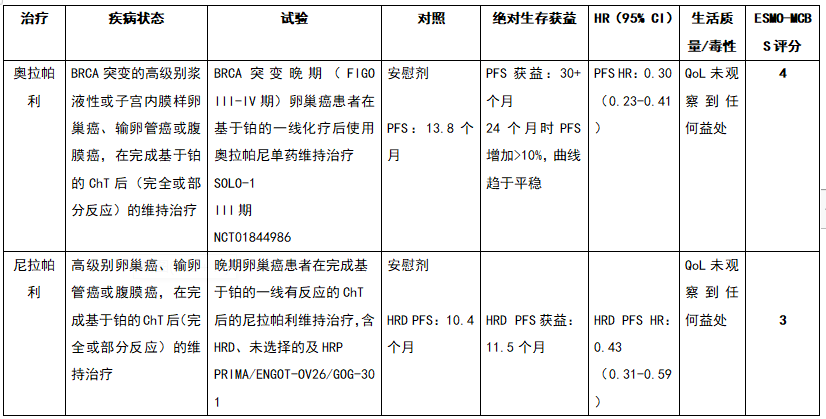
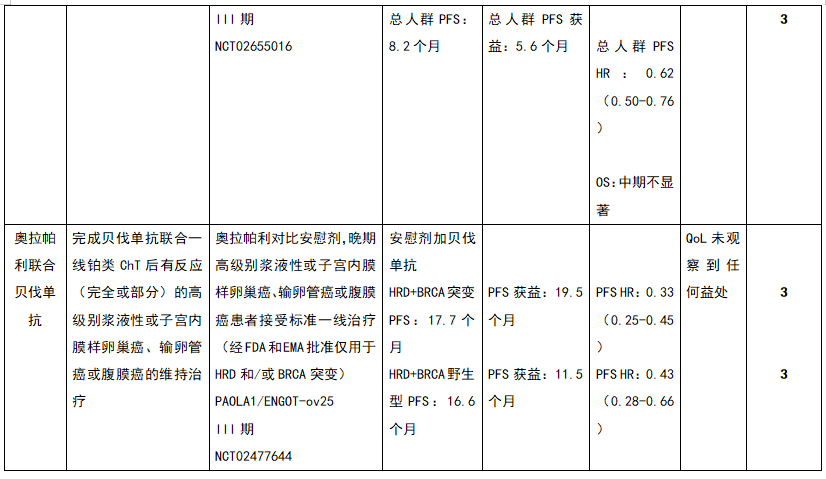

新诊断的上皮性卵巢癌新疗法/适应症的 ESMO-MCBS 表
注:BRCA,乳腺癌基因;ChT,化疗;CI,可信区间;EMA,欧洲药品管理局;ESMO-MCBS,ESMO临床获益量表;FDA,食品和药物管理局;HR,风险比;HRD,同源重组缺陷;ITT,意向性治疗;HRP,同源重组精通(HRD阴性);OS,总生存期;PFS,无进展生存期;QoL,生活质量。
✩ 本文仅供医疗卫生等专业人士参考
策划:GoEun,梅浙
投稿及合作:yinqihang@dxy.cn
题图来源:站酷海洛PLUS
参考文献
[1] Colombo N, Ledermann JA, on behalf of the ESMO Guidelines Committee, Updated treatment recommendations for newly diagnosed epithelial ovarian carcinoma from the ESMO Clinical Practice Guidelines, Annals of Oncology (2021), doi: https://doi.org/10.1016/j.annonc.2021.07.004.
[2] Ledermann JA, Raja FA, Fotopoulou C et al. Newly diagnosed and relapsed epithelial ovarian carcinoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up[J]. Ann Oncol. 2013,24 (Suppl 6): vi24-vi32.
[3] Moore K, Colombo N, Scambia G, et al. Maintenance olaparib in patients with newly diagnosed advanced ovarian cancer[J]. N Engl J Med,2018,379(26):2495-2505.
[4] González-Martín A, Pothuri B, Vergote I, et al. Niraparib in patients with newly diagnosed advanced ovarian cancer[J]. N Engl J Med, 2019,381(25):2391-2402.
[5] Ray-Coquard I, Pautier P, Pignata S, et al. Olaparib plus bevacizumab as first-line maintenance in ovarian cancer[J]. N Engl J Med, 2019,381(25):2416-2428.
[6] Coleman RL, Fleming GF, Brady MF, et al. Veliparib with first-line chemotherapy and as maintenance therapy in ovarian cancer[J]. N Engl J Med, 2019,381(25):2403-2415.
