2020 年 11 月 19 日,中国国家药品监督管理局(NMPA)官网显示,PD-1 免疫检查点抑制剂帕博利珠单抗注射液(商品名:可瑞达 ®)的一个新适应证的上市申请(受理号:JXSS2000010 国)状态已从「在审评审批中」转为「在审批」,意味着该适应证申请已完成技术评审,进入行政审批流程,有望在近期获批。
据悉,帕博利珠单抗(国内俗称「K 药」) 此次即将获批的适应证为一线治疗复发或转移性头颈部鳞癌(r/m HNSCC)。该适应证上市申请于今年 5 月 1 日获得 NMPA 的正式受理。
一旦获批,K 药在国内获批的一线治疗适应证将达到 4 个。K 药于 2019 年在局部晚期和/或转移性鳞和非鳞非小细胞肺癌(NSCLC)治疗领域连续获批 3 个一线治疗适应证。

2019 年 6 月 11 日, 美国 FDA 基于 3 期多中心、随机对照的 KEYNOTE-048 临床研究结果同时批准 2 个 K 药一线治疗 HNSCC 的适应证:
1. 联合化疗(含铂化疗和 5-FU)一线治疗 r/m HNSCC;
2. 单药一线治疗 PD-L1 阳性(CPS ≥ 1)的 r/m HNSCC。
欧盟和日本药品监管机构也基于 KEYNOTE-048 研究结果于 2019 年 11 月和 12 月相继批准 K 药联和化疗,以及单药一线治疗 r/m HNSCC。
仅凭一个 3 期临床研究即获批两个一线适应证的案例在免疫药物的研发中至今独一无二。KEYNOTE-048 有什么不同?
KEYNOTE-048 的「一打三」
2008 年 EGFR 靶向治疗药物西妥昔单抗联合含铂化疗和 5-FU(EXTREME 方案)一线治疗 r/m HNSCC 在全球获批,成为一线治疗 r/m HNSCC 的标准治疗方案 1。今年 3 月,该方案在国内也获批一线治疗 r/m HNSCC。
在 KEYNOTE-048 研究中,帕博利珠单抗没有效仿其在晚期 NSCLC 临床研究中选择与一线化疗方案作为对照,而是「更大胆」地直接选择与靶向药物联合化疗的三药联合方案直接「PK」3。
KEYNOTE-048 研究入组了 882 例复发或转移性头颈部 (口咽, 口腔, 下咽, 喉)的鳞状细胞癌患者,随机接受 K 药单药、K 药联合化疗或 EGFR 靶向药物西妥昔单抗联合化疗的方案,同时免疫和靶向治疗药物在化疗结束后作为维持治疗 2。
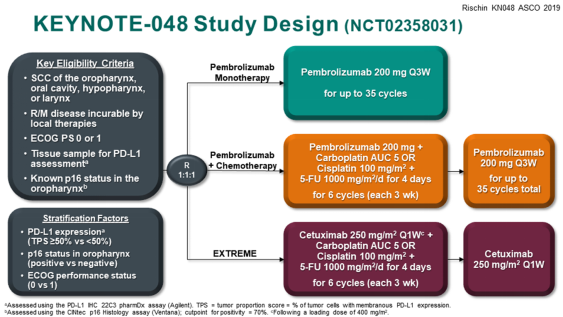
KEYNOTE-048 研究设计 2
该研究针对 PD-L1 CPS ≥ 20、CPS ≥ 1 和全体患者这 3 组人群,采用总生存(OS)和无进展生存(PFS)作为共同的主要终点。
疗效和安全性对决 - 免疫完胜靶向
研究结果显示,在 CPS ≥ 20 的人群中,K 药单药组与西妥昔单抗联合化疗组相比,中位 OS 分别为 14.8 个月(11.5~20.6)和 10.7 个月(8.8~12.8),HR = 0.58(95%CI 0.44~0.78),P = 0.0007, 死亡风险降低 42%;24 个月的 OS 分别为 35.3% 和 19.1%。
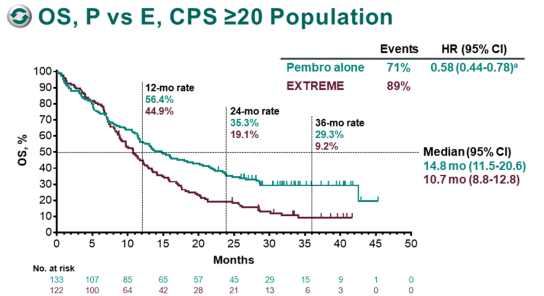
KEYNOTE-048:K 药单药对比靶向联合化疗一线治疗 PD-L1 CPS ≥ 20 r/m HNSCC 的 OS 2
在 CPS ≥ 1 的人群中,K 药单药组与西妥昔单抗联合化疗组相比,中位 OS 分别为 12.3 个月(10.8~14.3)和 10.3 个月(9.0~11.5),HR = 0.74(95%CI 0.61~0.90),P = 0.0086,死亡风险降低 26%;24 个月的 OS 分别为 28.9% 和 17.4%。
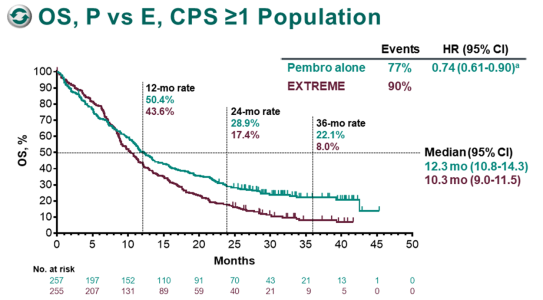
KEYNOTE-048:K 药单药对比靶向联合化疗一线治疗 PD-L1 CPS ≥ 1 r/m HNSCC 的 OS 2
在总人群中,虽然 K 药单药一线治疗仅显示非劣效于西妥昔单抗联合化疗组,但其联和化疗一线治疗方案却显示了显著优势:
K 药单药与西妥昔单抗联合化疗组相比,中位 OS 分别为 11.5 个月(10.3~13.4)和 10.7 个月(9.3~11.7),HR = 0.83(0.70~0.99),P = 0.0199。
K 药联和化疗与西妥昔单抗联合化疗组相比,中位 OS 分别为 13 个月(10.9~14.7)和 10.7 个月( 9.3~11.7),HR = 0.72(95%CI 0.60~0.87),P = 0.0034,死亡风险降低 28%。
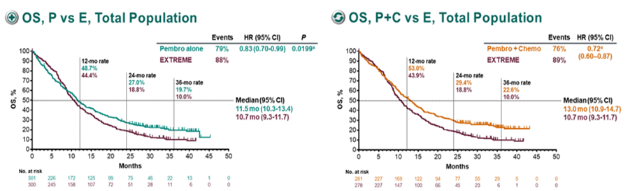
KEYNOTE-048:K 药单药及其联合化疗对比靶向联合化疗一线治疗整体人群 r/m HNSCC 的 OS 2
在毒性方面,K 药单药组在任意不良事件、3-5 级不良事件、不良事件导致死亡或停药的发生率均显著低于西妥昔单抗联合化疗组。
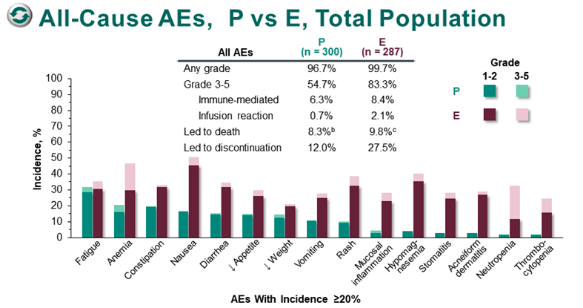
KEYNOTE-048:K 药单药对比靶向联合化疗一线治疗 HNSCC 的不良反应 2
而 K 药联合化疗组在任意不良事件、3-5 级不良事件、不良事件导致死亡或停药的发生率皆与西妥昔单抗联合化疗组相当。
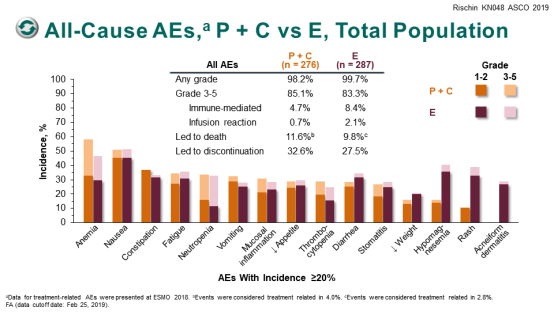
KEYNOTE-048:K 药联合化疗对比靶向联合化疗一线治疗 HNSCC 的不良反应 2
长生存的对决 -免疫完胜靶向
在今年 9 月结束的欧洲肿瘤内科学(ESMO)大会上,KEYNOTE-048 的四年随访总生存(OS)数据结果发布 3。结果显示,相比抗西妥昔单抗联合化疗方案,K 药单药一线治疗 PD-L1 表达阳性(CPS ≥ 1 和 CPS ≥ 20)的 r/m HNSCC,以及联合含铂化疗一线治疗 PD-L1 表达阳性人群和整体人群带来的四年总生存率都显示具有统计学意义和临床意义的优势。相比西妥昔单抗联合化疗方案,四年 OS 率提高了 3-5 倍 3。
针对 CPS ≥ 20% 的人群,K 药单药组的四年 OS 率达到 21.6%,是西妥昔单抗联合化疗方案(8.0%)的 2.7 倍;K 药联合化疗组的四年 OS 率可以达到 28.6%,是西妥昔单抗联合化疗方案(6.6%)的 4.3 倍;
在 CPS ≥ 1 人群中,K 药单药组的四年 OS 率为 16.7%,是西妥昔单抗联合化疗方案(5.9%)的 2.8 倍;K 药联合化疗组的四年 OS 率可以达到 21.8%,是西妥昔单抗联合化疗方案(4.1%)的 4.3 倍;
在总体人群,K 药单药组的四年 OS 率也达到 15.4%,是西妥昔单抗联合化疗方案(6.6%)的 2.3 倍;K 药联合化疗组的四年 OS 率为 19.4%,是西妥昔单抗联合化疗方案(4.5%)的 4.3 倍;
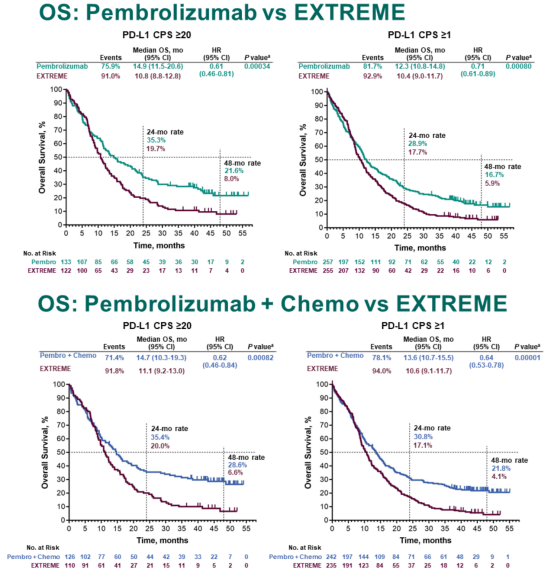
KEYNOTE-048:K 药单药,及其联合化疗一线治疗 CPS ≥ 20 和 CPS ≥ 1 人群的四年 OS3
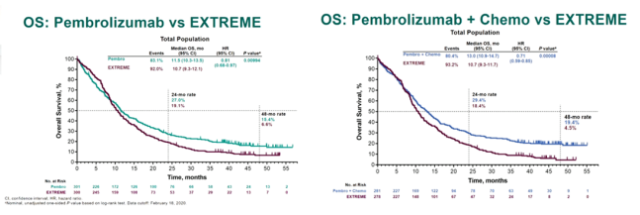
KEYNOTE-048:K 药单药,及其联合化疗一线治疗整体人群的四年 OS3
65% 的 HNSCC 会复发或转移,而对于局部复发的 HNSCC,再手术,放疗或两者联合的预后很差,与已出现远端转移的 HNSCC 相差无几。然而,化疗方案的选择非常有限,且预后不佳,5 年生存率不足 5%;即使联合了西妥昔单抗,四年的 OS 率也仍仅在 5%(4.5%-6.6%)左右 3。
K 药,及其联合化疗一线治疗的方案把整体人群的四年生存率提高了 9%-15%,把 PD-L1 表达阳性人群(CPS ≥ 20%)的四年生存率提高了 14%-22%,这必将有助于实现在 2030 年前提升头颈部鳞癌的五年生存率 15% 的目标。
参考文献
1.Laura QM Chow, Head and Neck Cancer, N Engl J Med 2020;382:60-72.
2.Burtness B, Harrington KJ, Greil R,et al. Pembrolizumab alone or with chemotherapy versus cetuximab with chemotherapy for recurrent or metastatic squamous cell carcinoma of the head and neck (KEYNOTE-048): a randomised, open-label, phase 3 study. Lancet. 2019 Oct 31. pii: S0140-6736(19)32591-7.
3.Brahmer JR,et al.KEYNOTE-024 5-year OS update:First-line(1L) pembrolizumab(pembro) vs platinum-based chemotherapy(chemo) in patients(pts) with metastatic NSCLC and PD-L1 tumour proportion score (TPS) ≥ 50%[EB/OL].ESMO 2020,abstract LBA51
