
2020 年 6 月 19 日,中国国家药品监督管理局(NMPA)官网显示,PD-1 免疫检查点抑制剂帕博利珠单抗(商品名:可瑞达®, 俗称「K 药」)一项适应证申请(受理号:JXSS1900044)赫然在列「2020 年 06 月 19 日药品批准证明文件待领取信息」名单中 1。
该受理号所对应的适应证为 K 药用于既往一线全身治疗失败的、局部晚期或转移性食管鳞状细胞癌(ESCC)患者的治疗。
这是 K 药在华获批的第五个适应证,居当前国内 8 个 PD-1/PD-L1 免疫检查点抑制剂获批适应证数量之首。
该适应证也将是 K 药在消化道肿瘤治疗领域获批的第一个适应证。目前 K 药在国内已获批二线治疗黑色素瘤,以及 2019 年在 8 个月内一口气「拿下」的三个一线治疗非小细胞肺癌(NSCLC)的适应证,包括联合化疗一线治疗转移性非鳞 NSCLC、联合化疗一线治疗转移性鳞状 NSCLC 以及单药一线治疗 PD-L1 表达阳性(TPS ≥ 1%)的局部晚期或转移性 NSCLC1。
12 个月生存率翻倍
该适应证的获批是基于一项全球多中心、开放标签、随机对照的 III 期临床研究 KEYNOTE-181 的结果。该研究结果首次于 2019 年美国临床肿瘤学会消化道肿瘤(ASCO-GI)年会上公布结果,并由北京大学肿瘤医院副院长,消化内科主任沈琳教授在 2019 欧洲肿瘤内科学学会(ESMO)年会上首次公布中国亚组人群的研究结果2。
KEYNOTE-181 研究共纳入了 123 例患者(119 例食管鳞癌)随机分配至帕博利珠单抗组(n = 62)和化疗组(n = 61);两组的中位随访时间分别为 15.1 个月和 14.7 个月。
结果显示,在意向治疗(ITT)人群和食管鳞癌人群中,K 药治疗组的中位总生存(mOS)都达到 8.4 个月,化疗组的 mOS 为 5.6 个月,死亡风险都降低 45%;ITT 和食管鳞癌人群 12 个月的生存率分别为 36% 和 35.7%,分别是化疗组(ITT 组, 17%;食管鳞癌,15.3%)的两倍多(看下图)2。
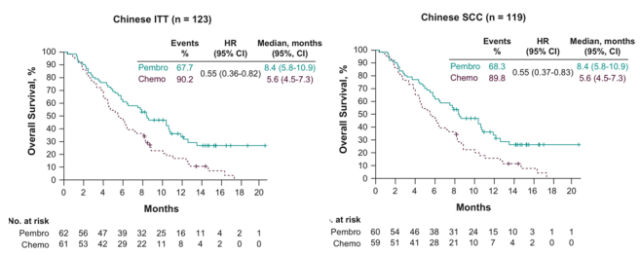
帕博利珠单抗治疗中国食管癌(ITT 和食管鳞癌人群)带来显著 OS 获益 2
中位 OS 突破 12 个月
而且在 PD-L1 表达阳性 (CPS ≥ 10)的人群中,相比化疗方案,K 药治疗中国人群的中位 OS 达到 12.0 个月,降低死亡风险 66%;在 12 个月时,超过一半的患者仍然存活,OS 率是化疗组的 3 倍多 2。
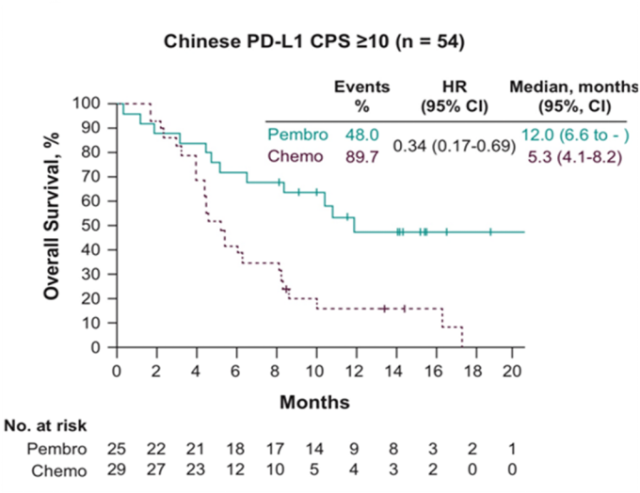
帕博利珠单抗治疗中国 PD-L1 表达阳性(CPS ≥ 10)食管癌带来显著 OS 获益 2
沈琳教授指出,食管癌治疗能带来中位 OS 超过 12 个月,近乎于化疗一线治疗能带来的 OS,这是食管癌治疗的一个历史性的突破;而且更重要的是,免疫治疗的疗效不仅限于 PD-L1 表达阳性的患者,因为 ITT 人群在帕博利珠单抗治疗后死亡风险也能降低 45%。
帕博利珠单抗组的与治疗相关的不良反应发生率低于化疗(K 药组 75.8%, 化疗组 83.1%),3-5 级不良反应的发生率更是仅有化疗组的一半 (K 药组 21.0%, 化疗 42.4%),而且也没有出现任何因脱靶而导致的反应性血管内皮细胞增生症(RCCEP)等不良反应。
50 年一遇的突破
我国食管癌的发病率和死亡率都居世界首位,食管癌新发患者和死亡患者的人数占全球的 55% 左右;而且我国食管癌五年生存率仅 15%-25%,背后的一个主要原因是我国约 70% 的患者在确诊时已为局部晚期或晚期转移性食管癌,失去了根治性手术机会,而多依赖化疗和/或放疗方案治疗。
而晚期转移性食管癌的治疗在过去几十年的发展缓慢,一线治疗仍以 5-FU,或紫杉醇联合含铂化疗为主,有效率低,中位的总生存不到一年;因此,约 60%-70% 的食管癌患者最终可能需要接受二线治疗,但二线治疗更是缺乏标准治疗方案。
KEYNOTE-181 是全球首个证实 PD-1 抑制剂疗效的大型三期临床研究,其中国亚组研究亦是首个公布的针对中国食管癌患者疗效的研究。K 药获批治疗晚期食管癌,意味着免疫治疗将成为我国食管癌二线治疗的新标准,从而打破食管癌系统治疗有效率低、副作用高疗效不尽人意的僵局。
参考文献
1.NMPA 官网
2. Chen J et al.,, Pembrolizumab versus Chemotherapy in Patients with Advanced/Metastatic Adenocarcinoma or Squamous Cell Carcinoma of the Esophagus as Second-line Therapy: Analysis of the Chinese Sub-group in KEYNOTE-181, Abstract, 2019 ESMO
