外科手术切除仍然是肝癌治疗的最有效的手段。经过数十年几代人的共同努力,肝癌根治性手术切除以及肝移植手术技术日趋精湛,我国肝癌病人的五年整体生存率也逐步由原来的 4.2% 提升到 12.5%1。
然而,这只是一个开始。
近年来,多个小分子多靶点抗肿瘤药物进入临床应用,多个 PD-1/PD-L1 免疫检查点抑制剂类药物的临床研究也取得了喜人的成果。
在系统治疗药物的推动下,我国中晚期肝癌的治疗模式正在发生巨大改变。在肝癌外科疗效提升速度减缓的情况下,肝癌围手术期的多学科综合治疗理念有望进一步提升我国肝癌的治疗水平,并延长患者的长期生存。本平台就此话题与华西医院肝脏外科肝脏移植中心主任文天夫教授和中山大学附属第三医院肝脏外科(肝脏移植)主任杨扬教授进行了深入的交流。
肝癌外科治疗的进展
文天夫教授:近两年,肝癌手术的术前评估与方案设计、术式选择、术后管理等方面都迅猛发展。随着影像学技术、微创外科、移植技术的发展和肝癌外科技术水平的提升,手术设计更为精准,患者的手术出血量、术后并发症都明显减少,因此外科治疗的安全性也得到了大幅提升。
但是肝癌根治性切除术后的总体 5 年复发率仍达 60% 左右,即便是小肝癌术后复发率也可达到 40%,最主要的原因就是恶性肿瘤的播散转移。中国 2003—2015 年的癌症统计数据显示,肝癌整体的 5 年生存率只有 12.5%,远低于邻国日本 60% 的肝癌五年生存率。
杨扬教授:肝癌系统治疗药物,尤其是多靶点小分子抗肿瘤药物在近几年的蓬勃发展拓宽了外科手术指征,让那些不可切除的晚期肝癌在肿瘤降期后转化为可手术切除,使以前不能治愈的晚期肝癌患者获得治愈的机会。另外系统治疗药物在预防肿瘤数目较多、肿瘤整体容积较大、合并微血管侵犯、大血管侵犯或Ⅱb 期以上的患者的术后复发,以及复发后的治疗的临床实践也在不断推进,这些都有望进一步提升肝癌手术后的生存率。肝癌治疗越来越依赖多学科综合治疗,越来越需要精准和个性化,这些新要求正在推动肝胆外科的变革。
一线治疗药物孰强孰弱
2007 年,随着多激酶抑制剂索拉非尼治疗不可切除晚期肝细胞癌适应证在国内获批,肝癌治疗迈入了靶向药物治疗时代。索拉非尼的疗效得到多个大型研究的支持,包括 SHARP、Oriental、Gideon 试验结果的支持。自 2007 年以后的十年间,其它靶向药物如血管生成抑制剂布利伐尼、舒尼替尼、多韦替尼,血管生成抑制剂利尼伐尼等用于晚期肝癌的临床试验均告失败,索拉非尼也因此一直是国内晚期肝癌治疗的一个标准。
REFELECT 研究是一项全球多中心、随机、开放的非劣效 III 期临床试验,共纳入 954 名既往未治疗的不可切除的 HCC 患者,其中包含近 300 例中国(大陆、台湾省、香港特区)患者,旨在评价一线应用仑伐替尼与当前标准治疗索拉非尼的疗效与安全性。
2017 年该研究的 III 期临床研究达到了主要研究终点,总生存(OS)非劣于索拉非尼,而在无进展生存期(PFS)、疾病进展时间(TTP)、客观缓解率(ORR)等方面仑伐替尼均显著优于索拉非尼(看下图)2。
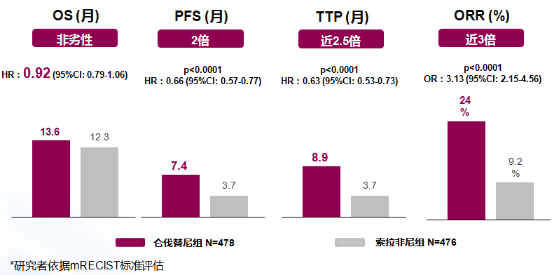
杨扬教授介绍,索拉非尼早期的研究主要是在西方患者中开展,对中国 HBV 相关的肝癌疗效并不十分理想;而在仑伐替尼Ⅲ期临床研究的亚组分析中,我们看到其对中国肝癌患者、HBV 相关肝癌的有效性明显优于索拉非尼,提示仑伐替尼更适合中国肝癌患者(看下图)。
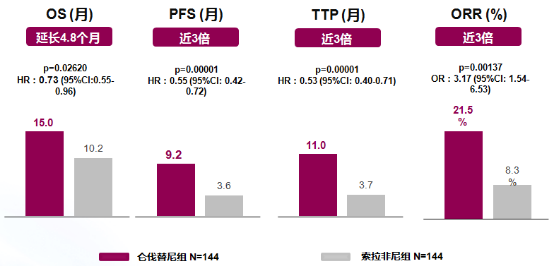
仑伐替尼于 2018 年 3 月在日本获批治疗肝细胞癌,2018 年 8 月在美国和欧洲获批该适应症;2018 年 8 月 4 日中国 CSCO 肝癌指南把仑伐替尼写进一线用药指南, 一个月之后(9 月 4 日)仑伐替尼在中国获批。
降期切除,好药早用
如何选择肝癌围手术期期间的系统治疗药物方案?文天夫教授认为,这要根据不同人群和不同治疗目标而定。
比如,对于不可切除的肝细胞癌的转化治疗,在选择系统治疗药物时,要根据 mRECIST 标准评估药物的客观缓解率(ORR),因为肿瘤的完全缓解(CR)或部分缓解(PR)的比例越高,就越有可能实现肝癌的降期,越有可能使肿瘤从不可切除转变为可切除。
而对于原发性肝癌根治性手术切除手术后的复发预防,选择系统药物时,则要根据 mRECIST 标准评估药物的疾病控制率(DCR),以及中位无复发生存期(mRFS)而最终极也是最重要的指标则是肿瘤治疗的金标准总生存(OS)。
2015 年 Lancet Oncology 刊登了对比肝癌切除术或者消融术后患者接受索拉非尼或者安慰剂的有效性及安全性的大型随机、双盲、对照的 III 临床研究(STORM)结果。 该研究随机选择 1,114 名患者入组。其中 556 名患者进入索拉非尼组,558 名患者进入了安慰剂组。81% 接受手术切除术,97% 为 Child-Pugh A,并且有 46% 存在高复发风险。结果显示索拉非尼组的最终中位无复发生存时间(RFS)与对照组无显著差异(索拉非尼组 33.3 个月对比安慰剂组 33.7 个月;HR 0.940;95% CI 0.780-1.134)3。
文天夫教授指出,该研究失败的原因可能有多种,包括研究人群的选择,东西方肝癌不同的认知不足,以及基础疾病的控制等,但有一个可能的原因是索拉非尼的客观缓解率较低,疾病控制率比较低。
「对于恶性肿瘤,尤其是肝癌这种恶性话程度很高的肿瘤,不应按照抗生素治疗的升阶梯治疗理念来用药,而是应该选择好药早用的策略,因为肿瘤患者生命时间窗口很短,如果错过了,疾病进展了,后续再用强效药,带来的生存获益自然就小了」,文教授认为,「尤其是在实行转化治疗的时候,更要选择高 ORR 的药物。」
联合治疗,提升 ORR
2019 年的欧洲肿瘤内科学学会(ESMO)大会和 ESMO-亚洲会议先后公布了仑伐替尼联合 PD-1 免疫检查点抑制剂帕博利珠单抗的 KEYNOTE-524/Study 116 开放标签单臂 Ib 期临床研究,以及 PD-L1 免疫检查点抑制剂阿替利珠单抗联合联合抗血管生成药物贝伐珠单抗一线治疗 HCC 的 IMbrave-150 III 期研究结果,结果令人振奋。联合治疗的 ORR 相比单药都有了进一步的提高。
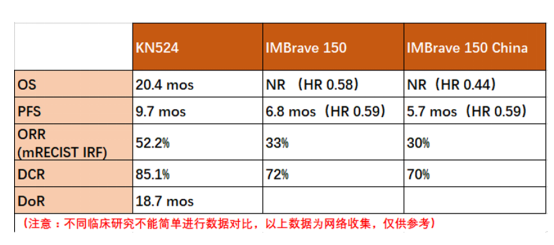
仑伐替尼联合帕博利珠单抗一线治疗晚期 HCC 的 ORR 达到 52.2%,疾病控制率 (DCR) 高达 85.1%4。
2019 年 7 月 23 日,美国 FDA 根据 KEYNOTE-524 的 1B 期研究结果授予仑伐替尼联合帕博利珠单抗一线治疗不适合局部治疗的晚期不可切除的 HCC 以突破性治疗方案(BTD)的指定,以加速该治疗方案的研发和注册。
杨扬教授认为,抗肿瘤靶向治疗药物与免疫治疗药物的「组合」在肝癌治疗领域具有巨大的潜力,为肝外科医生应对「狡猾」的肝癌带来了更多的「作战」选择方案,也将进一步促进肝癌的多学科综合治疗。
「目前临床上约 80% 肝癌患者不具备单纯外科手术的手术指征,这就更需要个体化治疗和多学科诊治」,杨扬教授指出,「对于早期肝癌患者,采用手术切除或者射频消融术联合免疫治疗药物进行辅助治疗,能够预防肿瘤复发,进一步改善患者生存;对于不可切除的肝癌患者,临床中已发现,抗肿瘤靶向药物或 PD-1/PD-L1 抑制剂与 TACE 的联合可以大大提高肝癌的治疗疗效;而对于既不可切除、又不能介入治疗的 HCC 患者,免疫治疗联合靶向药物治疗目前已显示出良好的应用前景」,杨扬教授相信通过以上多种治疗手段的联合,最终能够实现肝脏恶性肿瘤的全面控制。
参考文献
1.Zeng HM et al., Changing cancer survival in China during 2003–15: a pooled analysis of 17 population-based cancer registries, Lancet Global Health, 2018; 6: e555–67
2.Kudo, M., et al.,Lenvatinib versus sorafenib in first-line treatment of patients with unresectable hepatocellular carcinoma: a randomised phase 3 non-inferiority trial. Lancet, 2018.
3.Lancet Oncol.2015 年 9 月 8 日在线版
4.Ikeda M, Sung M W, Kudo M, et al. A phase Ib trial of lenvatinib (LEN) plus pembrolizumab (PEMBRO) in unresectable hepatocellular carcinoma (uHCC): Updated results. 2019 ESMO.
