原发性肝癌(简称「肝癌」)目前是全球范围内最常见的恶性肿瘤之一,而我国肝癌发病率、死亡率均居世界首位。据 2018 年发布的《中国肝癌大数据报告》显示,原发性肝癌全球每年新发病例 85.4 万,中国 46.6 万,约占全球的 55%[1]。目前,我国肝癌患者 5 年生存率仅为 12.5%,显著低于邻国日本,如何提高肝癌规范化诊疗水平、优化诊疗策略一直备受关注。
近日,在 2020 年首个肿瘤高峰论坛(「大默无限」MSD 肿瘤高峰论坛)上,记者采访了中国科学院院士、复旦大学附属中山医院院长樊嘉教授。樊嘉院士指出,近年来,系统治疗领域不同种类药物联合治疗策略的「逐渐绽放」,对肝癌突变靶点研究的深化,以及多学科合作,综合管理肝癌的理念的不断「进化」和「升级」,肝癌的治疗模式正在从根本上发生转变。毋庸置疑,这些进展必将让医生拥有更多的、更精准的治疗选择,从而提升我国肝癌的五年生存率。
「双剑合璧」- 免疫+靶向突破困境
系统治疗(或全身治疗)是提高肝癌疗效的一个最重要的组成部分。我国大多数肝癌患者在确诊时已属于进展期或晚期,肿瘤细胞在肝外存在广泛转移,肿瘤从早期局部发展为晚期全身的状态,因此,手术、放疗、介入等局部治疗手段难以满足临床治疗的需求 [2];这就需要依靠全身的系统治疗,即药物治疗来实现控制肿瘤、提高患者的疗效。
2019 年 12 月卫健委发布了《原发性肝癌诊疗规范(2019 年版)》,该规范针对系统治疗进行了重点更新。近年来,肝癌的系统治疗取得了突破性的进展,治疗药物不再是抗血管生成靶向药物索拉非尼一枝独秀。继瑞戈非尼奠定了索拉非尼治疗进展后的二线治疗地位后,2018 年公布的全球多中心 III 期临床研究 REFLECT 数据结果确定了仑伐替尼在肝癌一线治疗中的地位,仑伐替尼一线治疗不可切除肝细胞癌被国内外指南一致推荐 [3]。自此,肝癌的抗肿瘤靶向治疗有了更多选择。
近两年,免疫检查点抑制剂(ICI)在癌症治疗中 「风头正盛」,已获 FDA 批准治疗十多个恶性肿瘤。基于 CheckMate-040 和 KEYNOTE-224 研究,纳武利尤单抗和帕博利珠单抗获 FDA 批准用于晚期肝癌的二线治疗。2019 年美国临床肿瘤学会(ASCO)年会公布的 KEYNOTE-240 研究结果,进一步稳固了帕博利珠单抗的二线治疗地位 [4]。
但免疫单药治疗肝细胞癌的有效率仅在 20% 左右。在单药治疗效果有限的背景下,晚期肝细胞癌(HCC)的联合治疗是近年来临床研究的热点话题。仑伐替尼是各指南推荐的 HCC 一线治疗手段,帕博利珠单抗则在肝癌二线治疗中获得成功。仑伐替尼联合帕博利珠单抗治疗不可切除 HCC 患者的Ⅰb 期研究(KEYNOTE-524)初步结果显示,ORR(包括未经证实的缓解)为 44.8%(表 1),优于 REFLECT 试验的仑伐替尼组(24.1%);联合治疗组的中位 OS 为 20.4 个月,中位 PFS 为 9.7 个月 [5]。
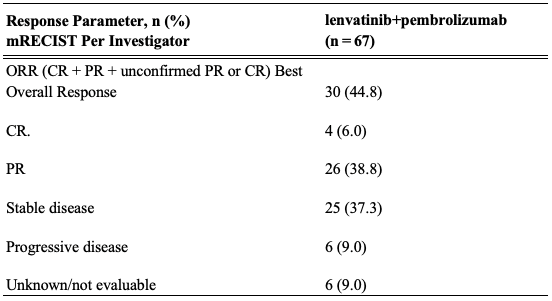
表 1. 肿瘤缓解情况
仑伐替尼联合帕博利珠单抗治疗展现了抗血管药物与免疫疗法联用的广阔前景。2019 年,在欧洲肿瘤内科学年会亚洲大会上 (ESMO-ASIA), PD-L1 单抗联合大分子抗血管生成单克隆抗体的 III 期临床研究 IMbrave-150 结果发布,得到了阳性结果,进一步提升了业界对免疫联合抗肿瘤靶向药物的期望。
但在肝细胞癌系统治疗中,能否像晚期非小细胞肺癌一样,找到更精准的靶点,并在此基础上研发出更精准的系统治疗药物?
精准分型 寻找肝癌新靶点
肝癌表现出的在时间和空间上的高度异质性为精准治疗策略的制订和实施增添了许多难题。
樊嘉院士指出,肝癌的发生和发展涉及多条信号通路的改变,每个癌细胞平均有 30~40 个突变,其中 5~8 种可能是驱动基因。目前也尚不能确定同一患者的每个癌细胞的驱动因子是否相同。当前的测序技术虽证实了原发及复发肿瘤的突变明显不同,但是肝癌的增殖和耐药机制会发生变异,这为找到固定的药物靶点带来挑战;因此,目前的精准医学还很难对肝癌进行分子病理水平的精准诊断和治疗,也就无法促进肝癌液体活检技术的应用和分子靶向药物的研发。
2019 年 10 月,樊嘉教授领衔团队,历时三年发现最新成果「乙肝相关肝细胞癌的整合蛋白质基因组学特征」刊于国际顶级生物医学期刊《细胞》[8]。研究首次揭示了我国肝癌与西方肝癌突变谱的不同,并提示肝癌患者按照分子分型可分为代谢驱动型、微环境失调型、增殖驱动型。分子分型的预后价值可能超过目前临床常用的表象分型。樊嘉院士认为,这三类亚型与基因组稳定性与基因突变、TNM 分期、肿瘤大小、癌栓有无、甲胎蛋白(AFP)及等临床特征都存在显著相关性(图 1)。
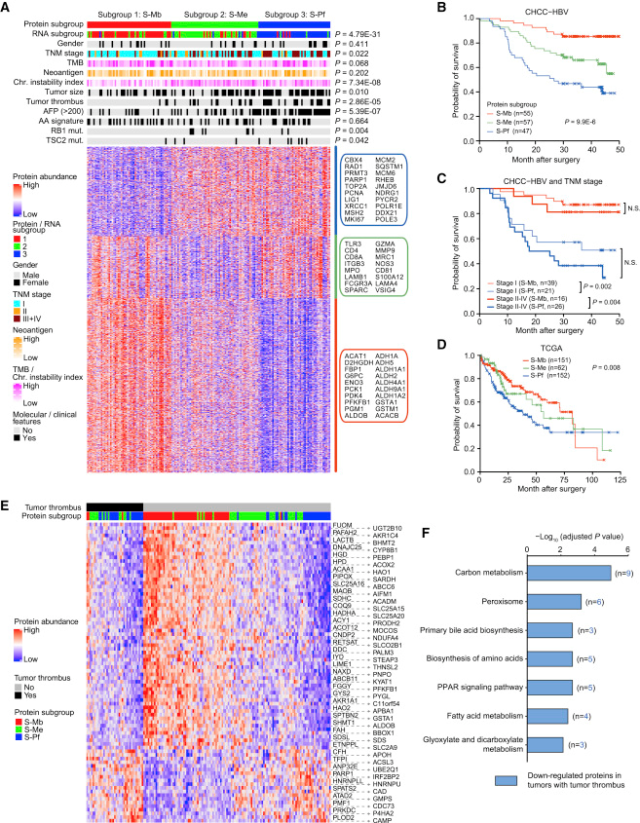
图 1 三个亚型与临床病理的相关性
樊嘉院士认为,如果要使分子靶向治疗成为肝癌治疗更有力的「武器」,为治疗有效率、生存获益等指标带来突破性的提升,寻找特定肿瘤分子标记物,选择敏感人群,从根本上实现量体裁衣的个体化治疗就势在必行 [9]。
除了个体化治疗,综合治疗也将是未来肝癌治疗的一个重要理念。 依据循证医学证据,针对患者的具体病情选择最合适的综合治疗方案,对提高肝癌的总体疗效和改善患者的预后具有重要意义 [6]。
樊嘉院士举例道,对不可切除的「晚期」肝癌,通过精准的术前辅助治疗方式来达到肿瘤「降期」的目的,让一部分不可切除患者转化为可切除;而对于具有高危复发风险的患者在外科术后进行精准预防,真正将肝癌的精准治疗思路集中在肝胆外科的临床转化上。
「精准治疗也意味着在临床上,应根据原发性肝癌患者的体力状况、肿瘤不同时期、肝癌分子分型、肝功能代偿程度、远处转移、血管侵犯以及肿瘤部位、数目和大小,针对具体病情和不同阶段采用个体化的、多学科综合治疗模式 (MDT)」,樊嘉院士强调。
精准+综合 让肝癌变慢病
多学科综合治疗是进一步提高肝癌治疗效果的重要组成部分,这是目前国内外学术界形成的重要共识。目前临床上约 80% 肝癌患者不具备单纯外科手术的手术指征,这就更需要个体化治疗和多学科诊治。多学科诊疗模式,包括肝外科、介入、肿瘤内科、放疗、肝病内科、影像、病理等多学科的协作。樊嘉院士指出,通过有效的 MDT 模式,肝癌患者可以从个体化,以临床证据为基础的临床治疗决策中受益:
■ 不能耐受或不适宜其他抗癌治疗但符合肝移植标准 , 可考虑肝移植;
■ 对小肝癌选择外科手术或消融治疗;
■ 对于下腔静脉癌栓患者,如因肿瘤压迫所致且无症状,可仅采用肝动脉化疗栓塞(TACE)治疗,观察肿瘤是否缩小;
■ 已有肝外转移的患者,以系统治疗为主,包括分子靶向治疗、免疫治疗、系统化疗、生物治疗和中医药治疗等。
免疫治疗与传统的手术、放疗或其他局部治疗联合也是未来的方向。樊嘉院士举例道,
■ 对于早期肝癌患者,采用手术切除或者射频消融术联合免疫治疗药物进行辅助治疗,能够预防肿瘤复发,进一步改善患者生存,目前已有相关研究正在进行中;
■ 对于不可切除的肝癌患者,临床中已发现,PD-1/PD-L1 抑制剂与 TACE 的联合可以大大提高肝癌的治疗疗效 [7];
■ 对于既不可切除、又不能介入治疗的 HCC 患者,免疫联合靶向药物治疗目前已显示出良好的应用前景。
最后,樊嘉院士强调,肝癌治疗不仅要探索精准医疗技术,更应强化精准理念。所谓的精准理念,即不能将所有肝癌患者的治疗一概而论,或治疗方式千篇一律化,要求临床医生从疾病的发生机制有根本认识,针对不同患者选择更具特异性、更有效的综合治疗方案。我们期待通过多种治疗手段的联合,最终能够实现肝脏恶性肿瘤的全面控制,实现肝癌的慢病化。
参考文献
[1] Cancer incidence and mortality in China, 2014. Chin J Cancer Res 2018;30(1).
[2] 郑小卫,王增,程斌. 晚期肝癌靶向药物治疗的临床研究进展 [J]. 中国药师,2012,15(1):107-109
[3] 李槐. 针对「瑞戈非尼用于索拉非尼治疗后进展的肝细胞癌患者 (RESORCE):一项随机、双盲、安慰剂对照Ⅲ期临床试验」导读 [J]. 肝癌电子杂志,2017,4(1):3-12.
[4] R. Finn, S.L. Chan, A.X. Zhu, et al. Pembrolizumab vs best supportive care for second-line advanced hepatocellular carcinoma: Randomized, phase 3 KEYNOTE-240 study[J]. Annals of Oncology, Volume 27, Issue suppl_6, 1 October 2016, 713TiP, https://doi.org/10.1093/annonc/mdw371.105
[5]Ikeda M, Sung M W, Kudo M, et al. A phase Ib trial of lenvatinib (LEN) plus pembrolizumab (PEMBRO) in unresectable hepatocellular carcinoma (uHCC): Updated results. 2019 ESMO.
[6] 叶胜龙. 原发性肝癌的多学科综合治疗 [A];《中华医学会第十六次全国病毒性肝炎及肝病学术会议论文汇编》[C];2013 年
[7]Shi L, et al. PD-1 Blockade Boosts Radiofrequency Ablation-Elicited Adaptive Immune Responses against Tumor. Clin Cancer Res[J]. 2016 Mar 1,22(5):1173-1184.
[8] Gao Q, Zhu H, Dong L, Shi W, Chen R, Song Z, Huang C, Li J, Dong X, Zhou Y, Liu Q, Ma L, Wang X, Zhou J, Liu Y, Boja E, Robles AI, Ma W, Wang P, Li Y, Ding L, Wen B, Zhang B, Rodriguez H, Gao D, Zhou H, Fan J. Integrated Proteogenomic Characterization of HBV-Related Hepatocellular Carcinoma. Cell, 2019 Oct 3;179(2):561-577.e22
[9] 李爱军,马森林,吴孟超. 分子靶向药物在肝癌治疗中的作用 [J]. 肝胆胰外科杂志,2015,27(3):255-257.
