如果说 2018 年是我国肿瘤免疫治疗的元年,那 2019 年无疑就是一线免疫治疗的元年,而且是收获颇丰的一年:国家药品监督管理局(NMPA)在不到 8 个月内批准了 PD-1 抑制剂帕博利珠单抗共计三个一线治疗非小细胞肺癌(NSCLC)的适应证1 ,使其成为名副其实的晚期 NSCLC 治疗的「一线 PD-1 单抗」,也让我国的晚期 NSCLC 治疗迅速、全面进入免疫一线的治疗时代,与欧美和日本等发达国家「齐肩」、并排走在前沿。
小编有幸在 2020 年首场国内肿瘤专家云集的肿瘤学术研讨大会上(「大默无限」- MSD 肿瘤高峰论坛)采访了同济大学附属上海肺科医院肿瘤内科主任周彩存教授以及上海交通大学附属上海胸科医院呼吸科主任韩宝惠教授。两位专家就免疫治疗的意义,免疫一线药物临床应用面临的挑战,以及免疫治疗的未来发展做了精彩的诠释和介绍。
免疫一线治疗的临床实践能否为我国晚期肺癌患者带来长期生存?
韩宝惠教授:2019 年获批的三个 PD-1 单抗一线治疗晚期 NSCLC 的适应证将改变驱动基因突变阴性的晚期 NSCLC 的治疗,其对于我国晚期 NSCLC 治疗的意义是巨大和深远的。

对改变临床实践贡献率和意义最大的是一线治疗的「升级换代」,因为,一线治疗对于改善和提升肿瘤患者总生存(OS)所占的权重比例是最大的;因此,夯实免疫作为一线基础治疗才能真正把任何 ORR 或 PFS 的优势转化为长期生存的优势。
帕博利珠单抗单药治疗晚期 NSCLC 的五年随访研究结果显示,一线治疗 PD-L1 高表达患者的五年总生存率达到近 30% 2,这是很了不起,在过去是难以想象的。 所以,如果能有更多的患者享受到免疫一线治疗,无论是单药还是联合化疗治疗方案,这些患者都有机会能获得长期生存的可能。
我们常说要把肺癌变成慢性病,那么在驱动基因突变阴性的 NSCLC 患者中,帕博利珠单抗的临床研究数据让我们看到了希望。 我们期待,在未来,会有更多的免疫一线治疗中国人群的长期随访数据,从而可以进一步推动我国晚期 NSCLC 治疗策略的「升级」。
编者注: 帕博利珠单抗治疗 NSCLC 的 KEYNOTE-001 的五年随访数据于 2019 年的美国临床肿瘤学年会公布,数据显示:
● 一线治疗 5 年总生存率(OS)为 23.2%(患者 101 例);
● 接受一线治疗的 PD-L1 高表达的患者(肿瘤表达评分 [TPS])≥ 50%), 生存率达到 29.6%3;
进入 2020 年,一线 PD-1 单抗在国内临床实践中的发展会遭遇哪些瓶颈?
能否成为一线治疗的新标准?
周彩存教授:在欧美和日本等发达国家, 免疫治疗已成为一线治疗晚期 NSCLC 的标准。 在三个一线治疗 NSCLC 的适应证获批后,在中国,一线免疫治疗也应该是临床实践的标准。

也就是说, 如果 PD-L1 表达高(TPS ≥ 50%), 帕博利珠单抗一线治疗是标准;其它病人,包括 PD-L1 表达阴性或表达的 TPS 值在 1%-49% 之间的患者,帕博利珠单抗联合化疗一线治疗的方案应该是当前的标准,因为,这样可使更多的病人获得长期生存的可能。KEYNOTE-001 的五年随访研究数据告诉我们, 帕博利珠单抗单药一线治疗晚期 NSCLC 的五年生存率在 23.2%, 其联合化疗一线治疗的五年生存率应该会更高,估计在 40%-50%,虽然最后的数据需要假以时日才能「出炉」。
但是在临床实践中,免疫一线治疗成为晚期 NSCLC 治疗的标准还要「翻过两座高山」。
第一座高山是一线治疗药物的可支付性目前仍然有限。
虽然当前有患者用药的援助项目(比如「生命之钥」),但这还不够;只有当这些一线治疗方案被医保覆盖后,当多数的国内患者能用得起一线治疗药物,免疫一线治疗才能真正成为临床实践的新标准。
另外一座高山是国内多数医生和患者对于免疫治疗仍然缺乏认知。
免疫治疗在国内起步比较晚,国内大城市的三甲医院的肿瘤/呼吸专科医生可能具备一定的认知,以及临床用药经验;而其它二线、三线城市医院的医生,尤其是基层医院的医生对免疫治疗的了解还相当有限,对免疫治疗引起的毒副作用比较担心,甚至恐惧。
所以,进入 2020, 我们要大力推广免疫治疗在医生和患者中的教育,让医生和患者免疫治疗带来的长期生存以及不良反应管理,这样才能让医生会用、敢用免疫治疗药物,从而让更多的国内 NSCLC 病人享受到免疫治疗可能带来的生的机会。
如何提升对免疫治疗的不良反应的认知并加强管控?不同 PD-1 单抗的毒副作用是否有所区别?
韩宝惠教授:目前的免疫治疗药物不像小分子靶向治疗药物那样毒副反应基本上都相似。比如在 EGFR-TKI 类药物中,无论是进口的还是国产的,其不良反应基本相同。但免疫治疗药物都是大分子的单克隆抗体,每个单抗都有独特的分子三维结构和生物学特性;在人体内,可能显示的就是不同的药物疗效和毒副反应。
所以经过这两三年的摸索,我们得出的结论就是此 PD-1 不等于彼 PD-1, 更不能等同于 PD-L1。 通过 KEYNOTE 研究系列得出的循证医学证据只适用于指导帕博利珠单抗的临床实践,不能延伸到其它的 PD-1 单抗。 这已是共识。
所以我们在临床实践中,就要收集每个 PD-1 单抗独特的毒副反应的信息。我们也已初步观察到,PD-1 单抗的毒副反应还是略有区别的,在管控上也不完全一样;而国内的 PD-1 单抗治疗晚期肺癌尚处于临床研究阶段,目前还没有适应证获批,还需要收集循证医学的证据,所以,我们还要进一步的研究和观察。
总体,每一个 PD-1 单抗,需要各自的循证医学证据,并给予仔细的分析和解读。
编者注:截至 2020 年 2 月 29 日,国内已获批的 PD-1/PD-L1 单抗已达到 8 个(6 个 PD-1 单抗,2 个 PD-L1 单抗),覆盖瘤种包括晚期 NSCLC、恶性黑色素瘤、经典型霍奇金淋巴瘤、III 期不可切除的 NSCLC,以及广泛期 SCLC。
周彩存教授: 当前,一、二线城市的三甲医院的肿瘤专科医生对于免疫治疗还是有一定认知的;可能三线、四线城市或基层医院医生对于免疫治疗的认知尚薄弱,也缺乏临床实践经验。
但是我想告诉大家的是,只要关注了免疫的毒副作用,大多数情况下,不良反应常见于皮肤,内分泌,消化道,而且大多数是可以管控的;心脏或神经系统的不良反应相当少见,即使碰到,若及时处理,仍然有管控的可能。 所以免疫治疗的不良反应并不可怕。
PD-1/PD-L1 单抗类药物越来越多,但每个药物不良反应若又不同,是不是很复杂?
周彩存教授: CSCO 已出台了免疫治疗的不良反应指南。所以,临床医生只要认识到各个 PD-1 之间是不同的,并在临床实践中关注到每个药物的不良反应,按规范治疗,并参考行业指南,就不会出大问题。
韩宝惠教授:从精准医学开始,靶向治疗就显示东西方人种对于 EGFR-TKI 的反应就有差异,为广大临床医生所关注。 KEYNOTE-407 和 KEYNOTE-042 研究结果都显示,帕博利珠单抗治疗中国人群的 PFS 和 OS 都要略优于其治疗高加索人种。 在临床实践中,我们应该关注这种差异。 但同时,东西方人种在免疫相关不良反应,比如典型肺炎、免疫性肠炎、免疫性内分泌失调的发生率上是否也会有所不同,我们也需要在临床实践中关注并收集信息。
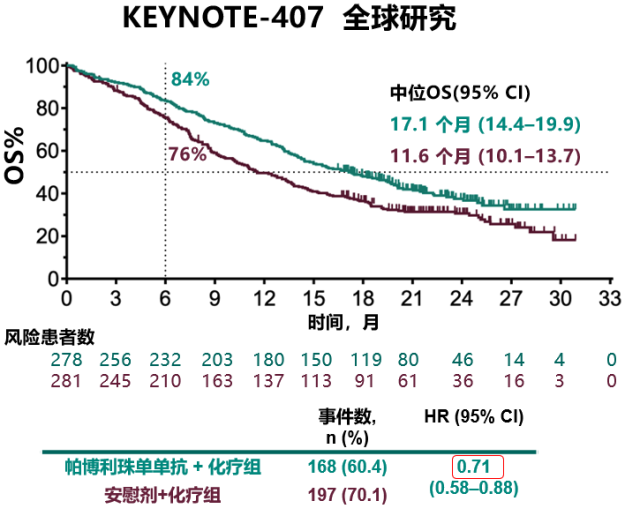
KEYNOTE-407 研究的 OS 数据结果显示帕博利珠单抗联合化疗一线治疗降低 29% 的死亡风险4
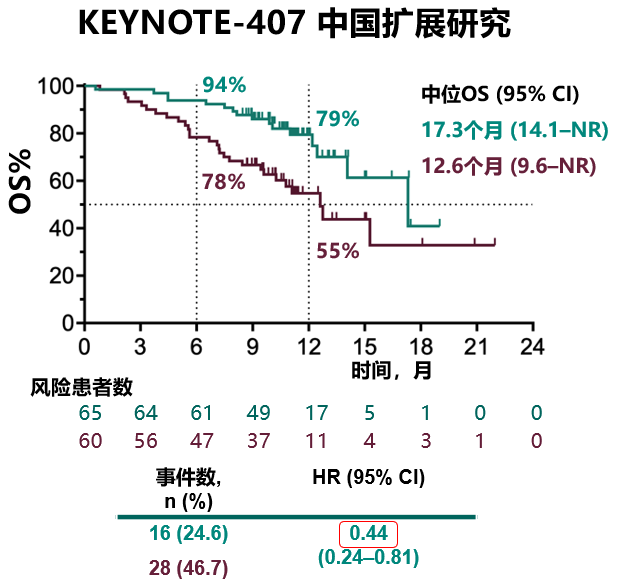
KEYNOTE-407 III 期临床研究中中国亚组 OS 数据结果显示帕博利珠单抗联合化疗一线治疗降低 56% 的死亡风险5
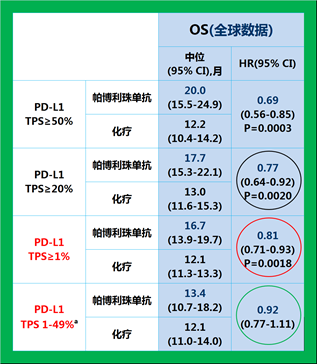
KEYNOTE-042 临床研究结果显示帕博利珠单抗单药治疗 PD-L1 表达阳性(TPS ≥ 1%) 的局部晚期或转移性 NSCLC 可降低死亡风险 19% 6
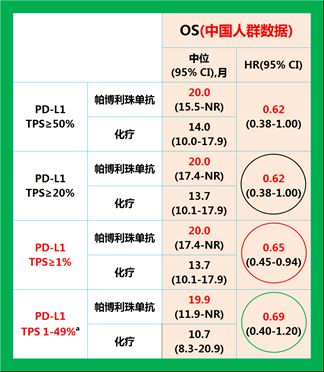
KEYNOTE-042 临床研究中国亚组及中国扩展研究结果显示帕博利珠单抗单药治疗 PD-L1 表达阳性(TPS ≥ 1%) 的局部晚期或转移性 NSCLC 可降低死亡风险 35% 7
免疫治疗可以带来长期生存,但是不是也会带来长期毒副反应? 需要担心吗?
周彩存教授:帕博利珠单抗的五年随访研究数据告诉我们,三年和五年的免疫相关的不良反应谱基本是一样的。 所以至少帕博利珠单抗的长期毒副反应是可预见的,大部分是可管控的。 这就让我们可以「放开手」, 在临床上至少给病人一个使用免疫一线治疗的机会,让一部分人可以长期生存,而这恰恰又是化疗或靶向药物治疗目前还无法做到的。
相比免疫单药治疗,化疗联合免疫的毒副反应如何?未来 NSCLC 治疗会否「去化疗」?
周彩存教授:很多患者选择免疫联合化疗一线治疗后发现,化疗有胃肠道反应以及毒性。但是选择帕博利珠单抗单药一线治疗又不一定符合 PD-L1 高表达(TPS ≥ 50%)的条件。但是有两类病人,即使 PD-L1 的表达水平比较高,我们还是主张要加化疗。
一类是肿瘤负荷比较大的病人,这类患者接受免疫联合化疗治疗的效果就会更好。 还有一类是肿瘤增长比较明显的病人,免疫加化疗是不错的选择,因为可以快速及时地控制住肿瘤的进展。
将来能不能有更多的病人享受到「无化疗」的治疗方案? 当前正在开展的免疫联合抗血管生成类药物的研究有望做到这点。 那时,我想适用人群范围可能会更广,对于 PD-L1 表达的要求更宽泛,比如,可能只要 TPS ≥ 20% 或 TPS ≥ 1% 就可以了,这样我们可以让更多的患者人群享受到「无化疗」治疗。但对于 PD-1 低表达,或者是不表达的患者,现阶段,免疫联合化疗可能还是最主要的治疗策略,因为 ORR, PFS 和 OS 都比化疗有所改善,不良反应虽然有所增加,但大部分还属于可管控范围。
韩宝惠教授:肺癌患者群体是一个复杂的群体,其中的一部分病人可能无法实现「去化疗」。肺癌治疗的复杂性、疾病表现的类型的多样性会制约医生最终选择的治疗方案,从而让选择的治疗方案有一定的局限性;所以任何一种治疗策略理念和观念都不可能实现人群全覆盖,可能都会有局限性,可能都仅能适用于一部分的患者人群。
比方说抗血管生成类药物联合 PD-1 单抗类免疫治疗药物的方案也有一定的局限性,因为抗血管类药物也有它的安全隐患,比如像鳞癌、有咯血的、靠近大血管的、有空腔……这些都是这类药物的禁忌,或相对禁忌;另外,对有高血压的,肾功能不好的患者,也不能使用抗血管相关的一些联合治疗。
因此,未来,肺癌治疗方案会更具多样性,而未来的临床实践一定是针对不同的患者,或在不同的情况下,选用最合适的方案。
所以,将来我们探索的领域还是非常多的。然而当前,免疫联合化疗一线治疗的循证医学证据是比较多,在现阶段,针对相当一部分病人,我们还是需要选择化疗作为免疫治疗的一个「搭档」。
参考文献
1.2019 年 3 月 28 日,国家药品监督管理局(NMPA)批准帕博利珠单抗联合培美曲塞和铂类化疗药物适用于 EGFR/ALK 基因突变阴性的转移性非鳞状 NSCLC 的一线治疗;
2019 年 9 月 29 日,NMPA 批准帕博利珠单抗适用于 PD-L1 表达阳性(TPS ≥ 1%)的 EGFR/ALK 基因突变阴性的局部晚期或转移性 NSCLC 一线单药治疗;
2019 年 11 月 22 日,NMPA 批准帕博利珠单抗联合卡铂和紫杉醇适用于转移性鳞状 NSCLC 的一线治疗。
2.Garon E et al., Five-Year Overall Survival for Patients With Advanced Non-Small-Cell-Lung Cancer Treated With Pembrolizumab: Results From the Phase I KEYNOTE-001 Study, Journal of Clinical Oncology, 2019.6.2
3.Garon EB, Hellmann MD, Rizvi NA, et al.Five-Year Overall Survival for Patients With Advanced Non‒Small-Cell Lung Cancer Treated With Pembrolizumab: Results From the Phase I KEYNOTE-001 Study[J]. J Clin Oncol. 2019; 37(28):2518-2527.
4.Paz-Ares et la., Pembrolizumab plus Chemmotherapy for Squamous Non-Small-Cell-Lung Cancer, N Engl J Med. 2018;379(21):2040-2051
5.Cheng Y et al.,KEYNOTE-407 China Extension Study: Pembrolizumab Plus Chemotherapy in Chinese Patients with Metastatic Squamous NSCLC, Oral Presentation, ESMO-Asia, 2019
6.Mok, T.S.K etal., Pembrolizumab versus chemotherapy for previously untreated, PD-L1-expressing, locally advanced or metastatic non-small-cell lung cancer (KEYNOTE-042): a randomized, open label, controlled, phase 3 trial. Lancet, April 4th, 2019
7.Wu Y.L et al., KEYNOTE-042 China Study: First-line Pembrolizumab vs Chemotherapy in Chinese Patients with Advanced NSCLC with PD-L1 TPS ≥ 1%, Mini-Oral Presentation, 2019 WCLC
*本采访由默沙东支持
本资料仅代表个人观点,仅作学术交流之用,请勿分发或转发
03-2021-CN-LAM-00040
