进入 2019 年的秋天,免疫治疗的三股旋风刮向我国的食管癌治疗,有望重塑我国食管癌的临床实践,并彻底改变治疗现状。
在第 15 届世界食管疾病大会(11 月 7 日-9 日)上,国内自主研发的 PD-1 单抗卡瑞利珠治疗食管鳞癌的随机 III 期临床研究(ESCORT)研究结果发布。而在一个多月前的 2019 年欧洲肿瘤内科学年会上(9 月 27 日至 10 月 1 日),纳武利尤单抗(O 药)二线治疗食管鳞癌(亚洲人群为主),以及帕博利珠单抗(K 药)治疗局部晚期和转移性食管癌的 III 期临床研究的中国人群数据(ATTRACTION-3 和 KEYNOTE-181)也公布了研究结果;KEYNOTE-181 研究的亚洲人群数据结果也于今年 9 月 19 日在中国临床肿瘤学会(CSCO)年会上公布。ESCORT, ATTRACTION-3 和 KEYNOTE-181 都显示了阳性结果,在这里我们就三个不同 PD-1 免疫检查点抑制剂的疗效和安全性做一个比较。
ESCORT 研究显示 PD-1 单抗带来显著 OS 改善 1
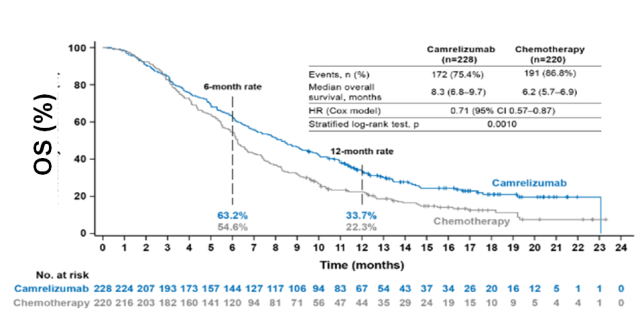
ESCORT 研究自 2017 年 5 月 10 日至 2018 年 7 月 24 日,共入组 457 例患者,随机接受卡瑞利珠单抗(200 mg,IV,每 2 周一次)或化疗,化疗方案包括多西他赛(75 mg/m2,IV,每 3 周一次)或伊立替康(180 mg/m2,IV,每 2 周一次)单药。两组患者的基线特征均衡。卡瑞利珠单抗组的中位随访时间为 8.3 (4.1-12.8) 个月,化疗组为 6.2 (3.6-10.1) 个月。
研究结果显示,同化疗方案相比,卡瑞利珠单抗组(228例)的中位总生存期(mOS)8.3个月,对比化疗组(6.2个月),延长2.1个月,降低死亡风险29%(HR=0.71[0.57-0.87] [2], 95% CI p=0.0010)。
[1] HR, Hazard Ratio 的缩写,指某一种干预措施(试验组)的应用所产生的风险率与不用该干预措施或者空白对照以及安慰剂等对照时所产生的风险率的比值。
自此,在国内获批的五个 PD-1 单抗中,已有三个 PD-1 单抗(除卡瑞利珠单抗外,还有帕博利珠单抗和纳武利尤单抗)在大型随机、对照 3 期临床研究中显示比化疗带来更优越的生存获益。
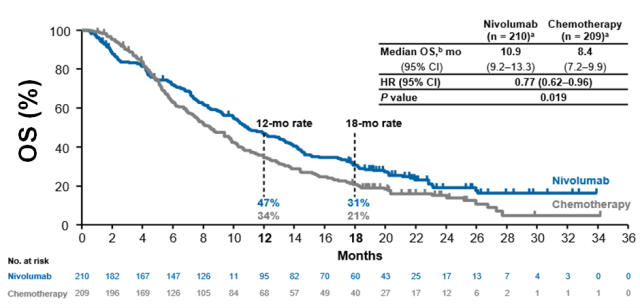
在今年的 ESMO 大会,纳武利尤单抗(O 药)单药治疗经治的不可手术切除的局部晚期和转移性食管鳞癌的 3 期临床研究 ATTRACTION-3公布研究结果。在入组的 419 例患者中,401 例来自亚洲,占 96%。 结果显示与化疗相比,纳武利尤单抗治疗组(240 mg, 每两周一次)的 mOS 为 10.9 个月(化疗组 8.4 个月), 延长 2.5 个月,死亡风险降低 23%(HR = 0.77[0.62-0.96], 95% CI,p = 0.019)2。
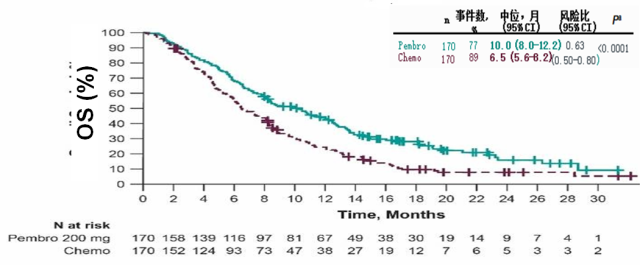
而在今年的 CSCO 大会上,由北京大学肿瘤医院副院长,消化内科主任沈琳教授牵头开展的帕博利珠单抗(K 药)单药治疗复发或转移性食管癌的全球多中心的 III 期临床研究 KEYNOTE-181 亚洲人群亚组的分析结果首次对外发布,结果显示,在食管鳞患者(96%的入组总例数)中,帕博利珠单抗组(200 mg 每三周一次)mOS 为 10.0 个月,较化疗组 6.5 个月,延长 3.5 个月,死亡风险降低 37%(HR 0.63[0.50~0.80];95%CI, p<0.0001)3。
三个 PD-1 单抗都改善 OS 但程度不同
对比数据显示,针对食管鳞癌患者,帕博利珠单抗(200 mg, IV, q3w)治疗带来的死亡风险降低幅度 最大,达到 37%, 而纳武利尤组(240 mg, IV, q2w)的死亡风险降低幅度最低, 仅 22%,卡瑞利珠(200 mg, IV, q2w)的 29% 处于中间。相比化疗,帕博利珠单抗治疗提升了 12 个月的生存率 19.3%,达到 43.5%,纳武利尤单抗提升了 13%, 卡瑞利珠为 11.4%。

在 PD-L1 表达阳性(CPS ≥ 10)的患者中,帕博利珠单抗治疗组的 mOS超过一年(12.5 个月),是化疗组(6.0 个月)的 两倍(HR 0.52;95%CI 0.37~0.74, p<0001),死亡风险降低达到 48%,超过一半的患者在 12 个月时仍然存活(54.2%),相比化疗(22.8%),提升了 31.4%。北京大学肿瘤医院副院长、消化内科主任沈琳教授曾指出,通过系统药物治疗能让 mOS 超越一年在食管癌治疗中实属罕见,K 药的数据甚至已超越化疗一线治疗的 mOS。在今年ESMO大会上,沈琳教授公布了KEYNOTE-181研究中的中国患者亚组数据,在PD-L1表达阳性(CPS≥10)的患者中,帕博利珠单抗治疗组相对于标准化疗死亡风险下降66%,中位生存期延长达到惊人的6.7个月[5]。
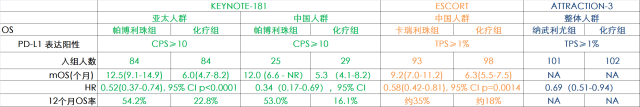
ESCORT 和 ATTRACTION-3 都选择在肿瘤细胞中的 PD-L1 表达 (TPS ≥ 1%,TPS 概念来定义 PD-L1 阳性人群。 卡瑞利珠单抗和 O 药治疗带来的死亡风险降低幅度都逊于 K 药;卡瑞利珠单抗的 mOS 为 9.2 个月,死亡风险降低 42%,12 个月 OS 率约 35%,相比化疗提升约 17%。而 ATTRACTION-3 研究仅公布了 O 药治疗降低了 31% 的死亡风险。
K 药凭借 KEYNOTE-181 研究结果于今年 7 月已在美国获批治疗食管癌的适应症,是目前全球唯一一个获批治疗食管癌的 PD-1 单抗。
最大的差异是安全性
但三个 PD-1 单抗之间 最大的差异还是在其在各自的临床研究中所展示的不良反应发生率。
K 药和 O 药都显示了比化疗方案更低的治疗相关不良反应发生率,但卡瑞利珠单抗的治疗相关不良反应发生率却要 高于化疗组(94.3% vs 90.0%)。
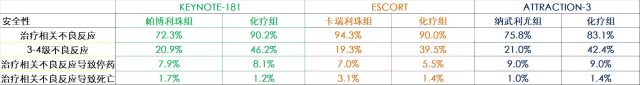
值得注意的是,与化疗相比,除了反应性毛细血管增生症(RCCEP)之外,几乎在其它所有不良反应发生率上,卡瑞利珠单抗组都要低于化疗组。唯独RCCEP(反应性毛细血管增生)的发生率高达 79.6%4; 而 KEYNOTE-181 和 ATTRACTION-3 研究都没有报道 RCCEP 的发生。
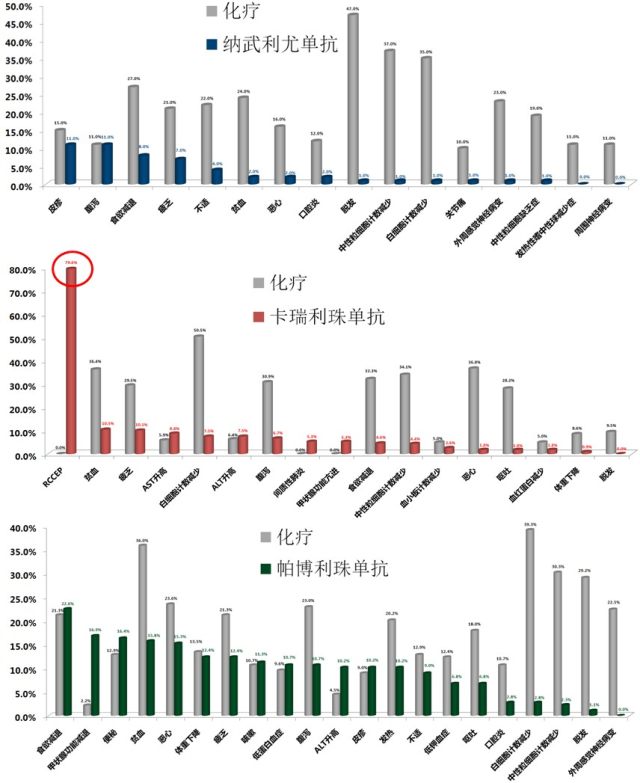
在 2018 年 ESMO 大会上公布的卡瑞利珠单抗二线治疗肝细胞癌的临床研究中,其治疗组的总体 RCCEP 发生率为 66.8%(q2w, 63.3%, q3w 70.4%)5。
今年 1 月,英国杂志《mAb》发表研究文章,指出可能是因为「脱靶」激活血管内皮生长因子受体 2(VEGFR2)的信号通路而导致独有的毛细血管增生引起的血管瘤的高比例发生。
VEGFR2 一般分布于血管和淋巴管内皮,其功能主要是调节淋巴管内皮细胞和血管内皮细胞,促进血管生成,还有促进淋巴管和调节淋巴细胞迁移等作用。目前已在国内上市的多个小分子抗血管生成药物,包括索拉非尼、舒尼替尼、瑞戈非尼、仑伐替尼等都能通过抑制 VEGFR2 信号传输通路来发挥抗肿瘤作用。
临床治疗上应如何抉择
食管癌是具有中国特色的肿瘤,发病人数占全球的一半,而且致死率高,是我国死亡率排名第四的恶性肿瘤。
但在过去几十年中,食管癌治疗的进展缓慢,在不可手术的局部晚期和转移性食管癌的治疗上更是严重缺乏有效的治疗手段。 在手术可切除的食管癌治疗上,虽然术前同步放化疗结合手术能提升 5 年生存率,但仍有超过一半的患者在术后有可能复发。
近几年,免疫治疗已改变了多个恶性肿瘤的治疗的临床实践。在国内,在晚期非小细胞肺癌(NSCLC)治疗领域,帕博利珠单抗已获批三个一线治疗适应症,纳武利尤单抗也获批二线治疗晚期转移性 NSCLC,多个国产 PD-1 单抗获批治疗经典霍奇金淋巴瘤,或不可切除的恶性黑色素瘤。今年我国可能还会迎来多个 PD-L1 单抗获批治疗 III 期不可切除的 NSCLC 和小细胞肺癌。明年,免疫治疗的光辉也将「照耀」我国的食管癌治疗(K 药和卡瑞利珠单抗治疗食管癌的适应症皆已获国家药品监督管理局受理)。
随着越来越多的 PD-1/PD-L1 单抗在国内进入临床应用,医生的临床实践必定会从最初的「粗狂」使用转型为「精细」思考,综合评估免疫治疗的疗效、安全性、方便性、患者依从性,以及药物价格。 在针对经常需要同步放化疗和手术联合治疗的早期和局部晚期食管癌患者时,安全性和可靠性自然成为除疗效之外的两个最重要,也是首当其冲要考量的因素。
[1] Huang J et al., Phase 3 study of camrelizumab vs chemotherapy for locally advanced/metastatic esophageal cancer: The ESCORT Study, Oral Presentation at the 15th OESO World Conference for Esophaeal Diseases, Nov. 7-9th, 2019
[2] HR, Hazard Ratio 的缩写,指某一种干预措施(试验组)的应用所产生的风险率与不用该干预措施或者空白对照以及安慰剂等对照时所产生的风险率的比值。
[3] Cho BC et al., Nivolumab Versus Chemotherapy in Advanced Esophageal Squamous Cell Carcinoma: The ATTRACTION-3 Study. Oral Presentation, ESMO Congress, September 27-October 1st, 2019
[4] Shen L et al., 帕博利珠单抗对比化疗二线治疗晚期/转移性食管腺癌或鳞状细胞癌: KEYNOTE-181亚洲亚组分析, 口头报告, 2019 CSCO, 9月18日-9月22日
[5] Chen J et al., Pembrolizumab Versus Chemotherapy in Patients with Advanced/Metastatic Adenocarcinoma or Squamous Cell Carcinoma of Esophagus as Second-line Therapy: Analysis of the Chinese Sub-group in KEYNOTE-181, Abstract Presentation, ESMO, September 27th, 2019
[6] Huang J et al., Phase 3 study of camrelizumab vs chemotherapy for locally advanced/metastatic esophageal cancer: The ESCORT Study, Oral Presentation, the 15th OESO World Conference for Esophaeal Diseases, Nov. 7-9th, 2019
[7] Qin SQ et al., A Randomized Multicentered Phase 2 Study to Evaluate SHR-1210 (PD-1 Antibody) in Subjects with Advanced Hepatocellular Carcinoma (HCC) who Failed or Intolerable to Prior Systemic Treatment, Oral Presentation, 2018 ESMO, Oct. 10, 018
