针对各种癌症的治疗指南目前已广泛应用于临床,然而这些治疗方案并非适用于每个患者,个体化的精准治疗依然任重道远。近日,浙江大学医学院附属第一医院郑树森教授团队将 MiniPDX 与二代测序结合,进行快速药敏试验的同时揭示关键基因的突变,为患者提供个体化治疗方案。相关成果发表于《Cancer Communications》。
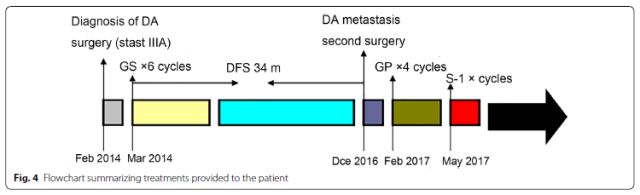
在该研究中, 一位十二指肠腺癌患者于 2014 年 2 月进行胰十二指肠切除手术,术后以常规方案吉西他滨联合 S-1 进行辅助化疗。于 2016 年 12 月 CT 复查显示其位于横结肠系膜下方的肠系膜上动脉根部出现转移灶,随后进行二次手术切除,并采用手术样本进行 MiniPDX 药敏试验。根据 MiniPDX 试验排序结果,采用吉西他滨联合顺铂进行术后辅助化疗。其后由于患者出现不适并依据 MiniPDX 试验排序结果调整为单药 S-1 治疗,在后期的九个月随访中,患者并未出现复发。该研究结果显示,患者的总体无疾病生存期可达 34 个月。而通常采用根治性切除手术的十二指肠腺癌伴随淋巴结转移的患者中位无疾病生存期在 18-25 个月,并且复发后生存时间仅为 5.4 个月。
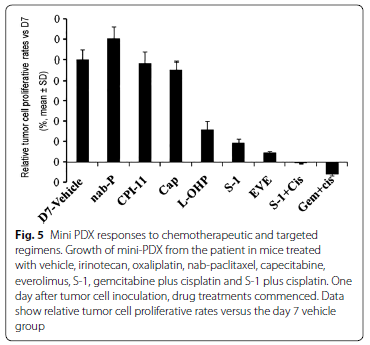
在本研究中,研究者同时还采用转移灶手术样本进行 WES/RNA 测序,证实转移性十二指肠腺癌出现了 KRAS 突变以及 TP53 和 RICTOR 扩增。RICTOR 是 mTORC2 复合物的重要组成部分,而 MiniPDX 结果也显示此患者对 mTOR 抑制剂依维莫司敏感。二代测序结果进一步佐证 MiniPDX 试验结果,表明如果此患者最终复发则可使用 mTOR 抑制剂进行治疗。
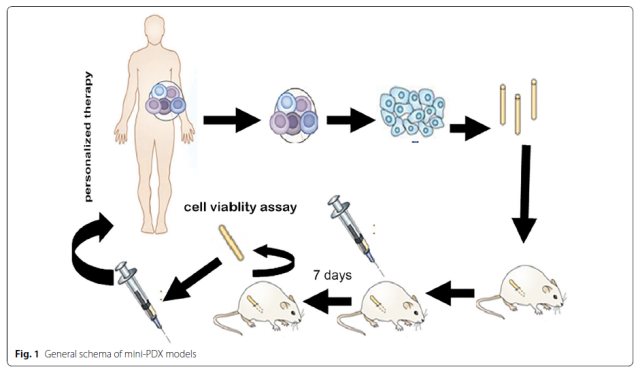
迷你人源性肿瘤移植动物模型(Mini patient derived xenograft, MiniPDX 模型)是采用特殊方法将原代人源肿瘤细胞移植在免疫缺陷小鼠身上后建立的一种药敏测试模型, 与 PDX 模型药敏检测相关性高达 92%, 相比于 PDX 药效试验,MiniPDX 周期短,仅 7 天即可完成药敏试验,可在短期内为患者提供个体化治疗方案, 是一种快速、经济、行之有效的体内药敏检测方法,对于晚期癌症的有效治疗具有很大的临床价值。
参考文献:
Peng Zhao, Hui Chen, Danyi Wen, Shuo Mou, Feifei Zhang and Shusen Zheng. Personalized treatment based on mini patient-derived xenografts and WES/RNA sequencing in a patient with metastatic duodenal adenocarcinoma. Cancer Commun (2018) 38: 54. https://doi.org/10.1186/s40880-018-0323-y
