肿瘤患者静脉血栓栓塞症 (VTE) 发生风险高,与非肿瘤患者相比,肿瘤化疗患者 VTE 风险增加 6 倍,肿瘤患者术后 4~12 个月 VTE 风险较普通人群增加 30 倍 [1,2]。肿瘤不同时期 VTE 复发风险不同,晚期或活动性肿瘤的 VTE 发生风险最高 [3]。
此外,VTE 是肿瘤患者第二大死亡原因,仅次于肿瘤本身 [4]。临床上亟需重视肿瘤相关血栓 (CAT) 的防治,尤其是活动性肿瘤患者的 VTE 防治。因此,我们邀请了马军教授为我们解读 CAT 抗凝治疗及利伐沙班在活动性肿瘤合并 VTE 治疗探索的最新研究 Select-D 研究。

CAT 的抗凝治疗
抗凝治疗是 CAT 的重要治疗措施之一,国内外权威指南一致推荐 CAT 患者至少抗凝 3 个月 [1,5-8]。2017 美国国家综合癌症网络 (NCCN) 指南 [5] 指出对于非导管相关的 VTE,如肿瘤处于活跃期、化疗中或复发的危险因素持续存在时,推荐无限期抗凝。
低分子肝素 (LMWH) 是指南推荐的 CAT 首选抗凝药物 [1,5-8]。然而,由于 LMWH 需要每日皮下注射、依赖与抗凝血酶 III(AT-III)起效、存在肝素诱导性血小板减少症 (HIT) 风险,限制了其在 CAT 治疗的应用。在真实的临床实践中,可见 CAT 患者 LMWH 长期依从性不足 50%[9],影响了 CAT 的有效治疗和预后。
利伐沙班在活动性肿瘤合并 VTE 治疗的探索
1、利伐沙班在活动性肿瘤合并 VTE 治疗探索的第一步:利伐沙班 vs LMWH 桥接 VKA
EINSTEIN PE/DVT 肿瘤亚组 [10],共纳入 655(8%) 例活动性肿瘤 (定义为在入选前 6 个月内发生的肿瘤,既往 6 个月内任何肿瘤治疗或复发性肿瘤或转移性肿瘤) 伴 VTE 患者,旨在比较利伐沙班单药与依诺肝素/VKA 治疗肿瘤伴 VTE 的疗效和安全性。结果显示,VTE 复发率两组相当;与依诺肝素/VKA 相比,利伐沙班显著降低活动性肿瘤伴 VTE 大出血风险达 58%(HR:0.42;95%CI:0.18-0.99),详见图 1。
2016 年美国胸科医师学会 (ACCP) 10 指南 [8] 推荐肿瘤相关 VTE,不能使用 LMWH 者,可使用新型口服抗凝药 (NOAC)(含利伐沙班)。目前,利伐沙班是惟一被欧盟药监局 (EMA) 认可,并批准用于治疗肿瘤相关 VTE 的 NOAC。
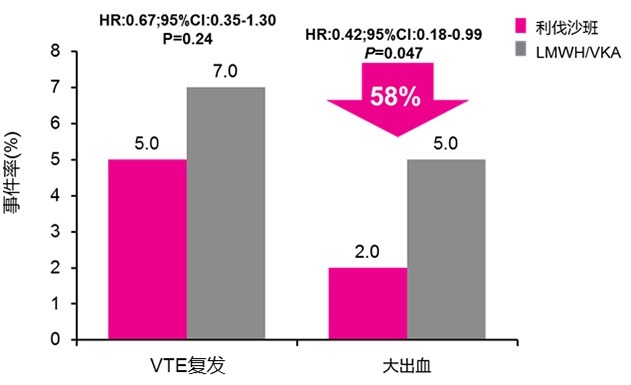
图 1 VTE 复发和大出血发生率
2、利伐沙班在活动性肿瘤合并 VTE 治疗探索的第二步:利伐沙班 vs 达肝素
Select-D 研究 [11] 作为第一项在 CAT 开展的 NOAC 与 LMWH 头对头研究,是一项前瞻性、随机、开放标签、多中心研究。旨在比较利伐沙班与达肝素在活动性肿瘤合并症状性 VTE 患者中的疗效和安全性。共纳入 530 例活动性肿瘤合并症状性 VTE 患者,随机分为达肝素组 (200 IU/kg i.h. 30 天后,150 IU/kg i.h.) 或利伐沙班组 (15 mg bid 21 天后,20 mg od)。两组转移性恶性肿瘤比例相同,均为 59%。利伐沙班组 PE 患者所占比例为 54%,达肝素组为 52%,详见 表 1。
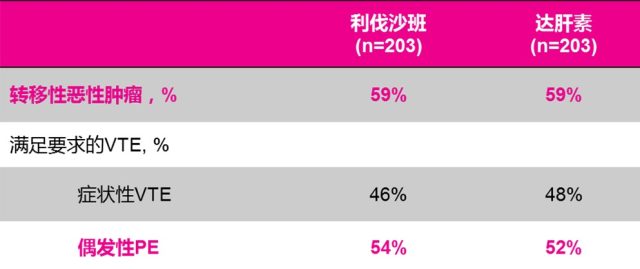
表 1 Select-D 研究:患者基线特征
Select-D 研究初步结果已在 12 月 12 日结束的 2017 美国血液病学会 (ASH) 年会上公布,结果显示: 与达肝素相比,利伐沙班用于治疗肿瘤合并 VTE 患者,VTE 复发率更低 (4% vs. 11%),详见图 2。在出血事件方面,利伐沙班大出血发生率为 5.4%,高于达肝素组 (2.9%);但致死性出血发生率相当,均为 0.5%,详见图 3。
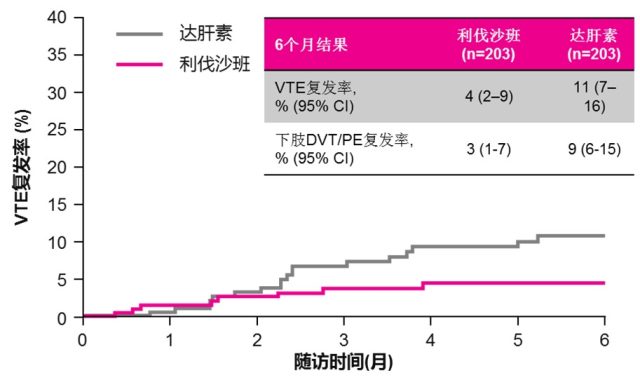
图 2 Select-D 研究:VTE 复发率
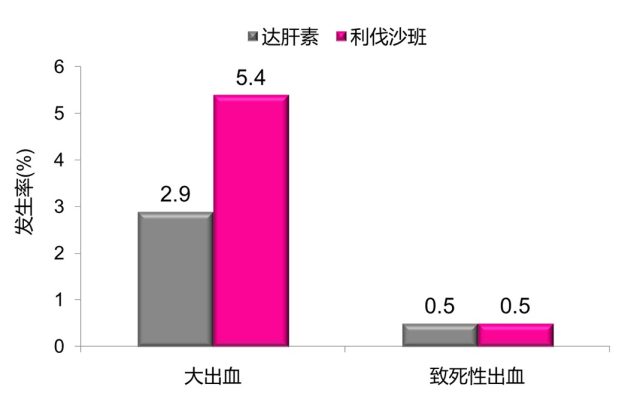
图 3 Select-D 研究:大出血和致死性出血发生率
综上所述,肿瘤患者 VTE 发生风险高,VTE 的发生影响肿瘤患者预后。LMWH 依赖 AT-III 起效、需要皮下注射、存在 HIT 风险,长期使用依从性不佳,影响了肿瘤患者 VTE 的规范治疗。直接 Xa 因子抑制剂,利伐沙班通过 EINSTEIN-cancer 和 Select-D 证实了利伐沙班用于治疗肿瘤相关 VTE 的安全性和有效性,是惟一被欧盟药监局 (EMA) 认可,并批准用于治疗肿瘤相关 VTE 的 NOAC。未来,利伐沙班将通过 CALLISTO 项目,进一步探索在 CAT 的防治中的临床价值。敬请期待!
参考文献:
1. 中国临床肿瘤学会肿瘤与血栓专家共识委员会《中国肿瘤临床》,2015,42(20):979-991.
2. Konstantinides SV, et al.Eur Heart J. 2014 Nov 14;35(43):3033-69, 3069a-3069k.
3. Streiff MB, et al. Clin Adv Hematol Oncol. 2013; 11(6): 349-57.
4. Khorana AA. Thromb Res. 2010;125(6):490-3.
5. NCCN. Cancer-Associated Venous Thromboembolic Disease. 2017
6. Lyman GH, et al. J Clin Oncol. 2013; 31: 2189-2204.
7. Farge D, et al. Lancet Oncol. 2016; 17: e452–66
8. Kearon C, et al. Chest. 2016; 149(2): 315-52
9. Mahé I, et al. J Thromb Haemost. 2016; 14(11): 2107-2113.
10. Prins MH et al, Lancet Haematol 2014;1:e37–e46.
11. Young A et al, ASH 2017: Abstract 625; Available at: http://www.clinicaltrialresults.org/
L.CN.MA.12.2017.4720
