在非小细胞肺癌的靶向治疗中,ALK 基因一直处于比较重要的地位,《NCCN 非小细胞肺癌临床实践指南》和《CSCO 原发性肺癌诊疗指南》都推荐含腺癌成分的非小细胞肺癌(NSCLC)患者常规进行 ALK 基因检测。
ALK 抑制剂:三国鼎立局面确立
携带 ALK 基因融合的 NSCLC 患者可以从 ALK 抑制剂中获益,克唑替尼(Crizotinib)自 2011 年在美国上市后,一直居于 ALK 基因融合阳性 NSCLC 一线治疗的霸主地位。二代 ALK 抑制剂色瑞替尼(Ceritinib)和 Alectinib 终于在 2017 年相继成功突围 ALK 阳性 NSCLC 一线治疗的领地,彻底改变了当前 ALK 阳性 NSCLC 的治疗格局,也带给我们新的思考。
科罗拉多大学胸科肿瘤科主任 David Ross Camidge 博士评论色瑞替尼的获批时表示,「色瑞替尼的获批标志着二代药物进入一线治疗的新战争打响了,这背后的逻辑可能是不必等到肿瘤进展到中枢神经系统抵抗或者进展,现在我们正在尝试尽早使用第二代 ALK 抑制剂」。
在 6 月 22 日更新的 《NCCN 非小细胞肺癌临床实践指南》(2017.V7)版本中,正式确立 Alectinib 为 ALK 阳性的 NSCLC 患者一线治疗的地位(1 级推荐),而且推荐顺序居然排在了克唑替尼、色瑞替尼之前。
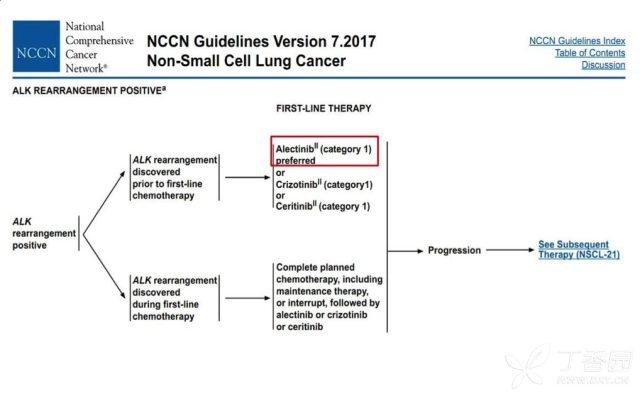
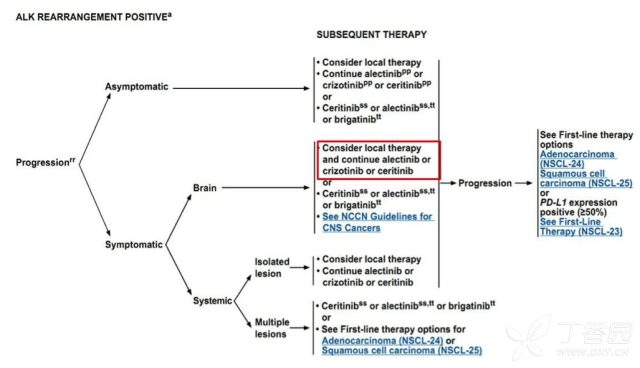
如今出现三国鼎立的局面,谁将更胜一筹?我们且来回顾一下历史重要事件。
Alectinib:后来者居上
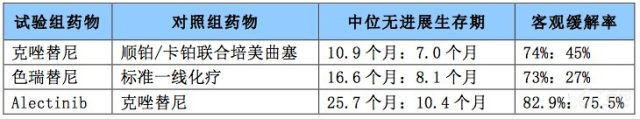
克唑替尼分别于 2011 年、2013 年通过 FDA 和 CFDA 批准,用于 ALK 基因融合阳性晚期 NSCLC 患者的治疗。PROFILE1014 研究共纳入 343 例 ALK 阳性的 NSCLC 患者,其中分别接受克唑替尼治疗和一线化疗(顺铂/卡铂联合培美曲塞)。相比于一线化疗组,克唑替尼组同样显示了较长的无进展生存期 PFS(10.9 个月对比 7.0 个月)和较高的药物缓解率(RR)(74% 对比 45%)。
色瑞替尼于 2014 年被 FDA 批准,用于既往接受克唑替尼后病情进展或对克唑替尼不耐受的 ALK 阳性晚期 NSCLC 患者的治疗。2017 年 5 月底,FDA 批准色瑞替尼用于 ALK 阳性的晚期 NSCLC 患者的一线治疗。FDA 的快速审批是基于 Ⅲ 期 ASCEND-4 临床研究的结果,该研究表明未接受过其他治疗的病人接受色瑞替尼治疗后的中位 PFS 为 16.6 个月,而接受化疗的病人的中位 PFS 仅为 8.1 个月。色瑞替尼组的药物缓解率为 73%,高于化疗组的 27%。《NCCN 非小细胞肺癌临床实践指南》(2017.V5) 开始推荐色瑞替尼作为 ALK 阳性的晚期 NSCLC 患者的一线治疗(证据等级 1)。
Alectinib 首先于 2014 年在日本上市,用于 ALK 阳性的的晚期 NSCLC 患者的治疗。在 2015 年年底,Alectinib 被 FDA 批准用于既往接受克唑替尼后病情进展或对克唑替尼不耐受的 ALK 阳性的晚期 NSCLC 患者的治疗。在 2017 年 ASCO 会议上,Alectinib 闪耀登场,大放光彩,与克唑替尼一线治疗的头对头的比较研究中,全面碾压了克唑替尼。《NCCN 非小细胞肺癌临床实践指南》(2017.V7)版本,正式确立 Alectinib 为 ALK 阳性的 NSCLC 患者一线治疗的地位(证据等级 1),后来者居上。
ALEX 研究:Alectinib 疗效出色
ALEX 临床研究是一项随机、开放的 Ⅲ 期临床试验,纳入了 303 例未经治疗的 ALK 阳性的 NSCLC 患者,其中包括中枢神经系统无症状进展的患者,随机分到克唑替尼组(250 mg/Bid)和 Alectinib 组(600 mg/Bid)进行治疗。在经过 17.6 个月(克唑替尼)和 18.6 个月(Alectinib)的中位随访时间后,Alectinib 组 12 个月时的 PFS 的比例高达 68.4%,而克唑替尼组的 PFS 的比例只有 48.7%。并且在 24 个月的时候,Alectinib 组的 PFS 的比例仍保持在 60% 左右,而克唑替尼组就仅有 20% 左右。
目前,Alectinib 组的中位 PFS 仍未达到。在此次试验中,Alectinib 在 NSCLC 伴中枢神经转移的患者中,同样表现相当出彩。12 个月时,Alectinib 组的中枢神经系统进展累积发生率仅为 9.4%,而克唑替尼组则为 41.4%。对于非小细胞肺癌伴中枢神经系统进展的患者,Alectinib 无论在一线或者二线治疗中都有出色的疗效。
此外,Alectinib 组的总生存期也优于克唑替尼组。Alectinib 组的药物缓解率为 82.9%,也高于克唑替尼组的 75.5%。安全性方面,3~5 级不良反应在 Alectinib 组为 41%,低于克唑替尼组的 50%。
一、二、三代 ALK 抑制剂现状
尽管大多数患者最初受益于克唑替尼,但肿瘤通常在治疗后 1 年内再次进展。目前较为明确的耐药机制主要分为 2 大类:一是 ALK 本身的变化,ALK 基因扩增或者 ALK 激酶结构域的继发耐药位点;二是旁路途径的激活,包括其他受体酪氨酸激酶的通路或细胞下游的信号通路。
此外血脑屏障的存在是不是克唑替尼的原发性耐药机制一直备受关注,约有 50% 的患者在接受克唑替尼治疗期间会发生中枢神经系统进展。二代或者三代 ALK 抑制一直在这些方面进行升级和改善。
表 1 不同 ALK 抑制剂一线治疗疗效对比
这些在研的 ALK 抑制剂中,也有诸多后起之秀。Lorlatinib 是一个第三代 ALK/ ROS1 抑制剂,低于纳摩尔的剂量就能有效抑制 EML4-ALK 基因重排,其独特的大环结构也使其有更好的血脑屏障穿透能力,目前也是唯一一个能克服 ALK-G1202R 耐药位点的 ALK 抑制剂。Lorlatinib 于 2017 年 4 月获 FDA 突破性疗法认法,用于 ALK 阳性的 NSCLC 患者的二线治疗。目前也有和克唑替尼比较用于 ALK 阳性一线治疗转移 NSCLC 患者的临床试验(NCT03052608)。
表 2 ALK 多靶点抑制剂列表
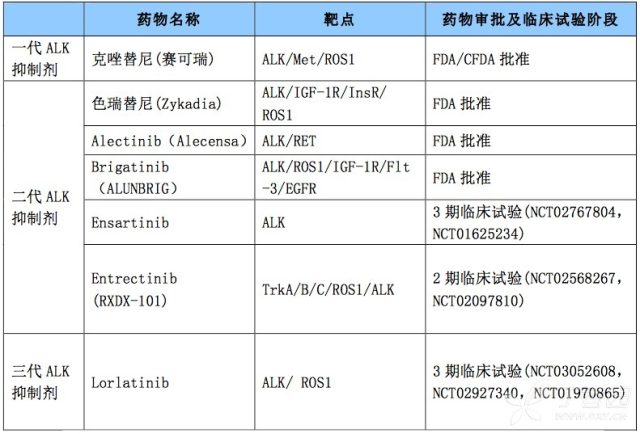
我们期待着新一代的 ALK 抑制剂可以为患者带来更好的治疗效果,也感谢药物开发者的智慧为生命带来新的希望。
参考文献
1. Solomon BJ, Mok T, Kim DW, et al. First-line crizotinib versus chemotherapy in ALK-positive lung cancer. N Engl J Med. 2014;371(23):2167-2177.
2. Soria JC, Tan DS, Chiari R, et al. First-line ceritinib versus platinum-based chemotherapy in advanced ALK-rearranged non-small-cell lung cancer (ASCEND-4): a randomised, open-label, phase 3 study. Lancet. 2017;389(10072):917-929.
3. Peters S, Camidge DR, Shaw AT, et al. Alectinib versus Crizotinib in Untreated ALK-Positive Non-Small-Cell Lung Cancer. N Engl J Med. 2017.
4. Toyokawa G, Seto T. Updated Evidence on the Mechanisms of Resistance to ALK Inhibitors and Strategies to Overcome Such Resistance: Clinical and Preclinical Data. Oncol Res Treat. 2015;38(6):291-298.
5. FDA Expands Approval of Ceritinib for ALK-Positive Non-Small Cell Lung Cancer.NIH. June 27, 2017.
